Telangana TSBIE TS Inter 1st Year Chemistry Study Material 10th Lesson P బ్లాక్ మూలకాలు – 13వ గ్రూప్ Textbook Questions and Answers.
TS Inter 1st Year Chemistry Study Material 10th Lesson P బ్లాక్ మూలకాలు – 13వ గ్రూప్
అత్యంత లఘు సమాధాన ప్రశ్నలు
ప్రశ్న 1.
బోరాన్, థాలియం ఆక్సిడేషన్ స్థితుల మార్పు విధానాన్ని చర్చించండి.
జవాబు:
IIIA గ్రూపు మూలకాల బాహ్య ఎలక్ట్రాన్ విన్యాసం ns2 np1. ఈ విన్యాసం వలన ఈ మూలకాలన్ని +3 ఆక్సిడేషన్ స్థితిని కనపరుస్తాయి. B, Al మినహా మిగిలిన అన్ని మూలకాలు +1 ఆక్సిడేషన్ స్థితిని చూపిస్తాయి. +3 ఆక్సీకరణ స్థితి యొక్క స్థిరత్వం B నుంచి Tl కు తగ్గుతుంది. +1 ఆక్సీకరణ స్థితి యొక్క స్థిరత్వం జడ ఎలక్ట్రాన్ జంట ప్రభావం వలన పై నుంచి క్రిందకు పెరుగుతుంది.
ప్రశ్న 2.
Tl Cl3 అధిక స్థిరత్వాన్ని ఎట్లా వివరిస్తారు ?
జవాబు:
TlCl3 అస్థిరమైనది జడ ఎలక్ట్రాన్ జంట ప్రభావం వలన Tl+3 అయాన్ అస్థిరమైనది. థాలియం +1 ఆక్సీకరణ స్థితిలో స్థిరంగా ఉంటుంది. కావున TlCl స్థిరమైనది.
![]()
ప్రశ్న 3.
BF3 లూయీ ఆమ్లంగా ఎందుకు ప్రవర్తిస్తుంది ?
జవాబు:
- BF3 ఎలక్ట్రాన్ కొరత గల సమ్మేళనం.
- అష్టక విన్యాసం పొందటం కోసం ఇది ఎలక్ట్రాన్ జంటను స్వీకరిస్తుంది.
- ఎలక్ట్రాన్ జంటల స్వీకర్తలను లూయీ ఆమ్లాలు అంటారు.
- కావున BF3 లూయీ ఆమ్లంగా ప్రవర్తిస్తుంది.
ప్రశ్న 4.
బోరిక్ ఆమ్లం ప్రోటాన్ ఇచ్చే ఆమ్లమా ? వివరించండి.
జవాబు:
- బోరిక్ ఆమ్లం ప్రోటాన్ ఇచ్చే ఆమ్లము కాదు. కాని ఇది లూయీ ఆమ్లంగా ప్రవర్తిస్తుంది.
- ఇది ఎలక్ట్రాన్ జంటను హైడ్రాక్సిల్ అయాన్ నుంచి స్వీకరించి లూయీ ఆమ్లంగా పనిచేస్తుంది.
B(OH)3 + 2HOH → [B(OH)4]– + H3\(\mathrm{O}^{+}\)
ప్రశ్న 5.
బోరిక్ ఆమ్లాన్ని వేడిచేస్తే ఏమవుతుంది ?
జవాబు:
బోరిక్ ఆమ్లాన్ని 370K కంటే ఎక్కువ ఉష్ణోగ్రతకు వేడిచేస్తే మెటాబోరికామ్లం (HBO2) ఏర్పడుతుంది. దీనిని ఇంకా వేడిచేస్తే బోరిక్ ఆక్సైడ్ (B2O3) ఏర్పడుతుంది.
![]()
ప్రశ్న 6.
BF3, B\(H_4^{-}\) ల ఆకారాలను వర్ణించండి. ఈ కణాలలో బోరాన్ సంకరకరణం రాయండి.
జవాబు:
- BF3 అణువు ఆకారం సమతల త్రిభుజాకారం. దీనిలో బోరాన్ sp2 సంకరీకరణం జరుపుకుంటుంది.
- B\(\mathrm{H}_4^{-}\) అణువు ఆకారం టెట్రాహెడ్రల్. దీనిలో బోరాన్ sp3 సంకరీకరణం జరుపుకుంటుంది.
![]()
ప్రశ్న 7.
Ga పరమాణు వ్యాసార్ధం Al కంటే ఎందుకు తక్కువ ఉంటుంది ? వివరించండి.
జవాబు:
- గాలియంలో ఉపాంత్యకర్పరంలో పది 3d – ఎలక్ట్రాన్లు ఉంటాయి.
- ఈ ఎలక్ట్రాన్ల వలన పరిరక్షక ప్రభావం తక్కువగా ఉంటుంది. కావున ‘Ga’ లో కేంద్రక ఆవేశం పెరుగును.
- కావున Ga యొక్క పరమాణు వ్యాసార్ధం Al కంటే తక్కువగా ఉంటుంది.
ప్రశ్న 8.
జడజంట ప్రభావాన్ని వివరించండి.
జవాబు:
బాహ్యస్థాయి (ns) లోని ఎలక్ట్రాన్లను విడగొట్టి బంధంలో పాల్గొనకుండా చేసే ప్రభావాన్ని జడ ఎలక్ట్రాన్ జంట ప్రభావం అంటారు.
ప్రశ్న 9.
ఈ క్రింది సమీకరణాలను తుల్యంచేసి రాయండి.
a) BF3 + LiH →
b) B2H6 + H2O →
c) NaH + B2H6
d)
![]()
e)
![]()
జవాబు:
a) 2BF3 + 6LiH → B2H6 + 6LiF
b) B2H6 + 6H2O → 2 H3BO3 + 6H2
c) 2NaH + B2H6 → 2 NaBH4
d)
![]()
e)
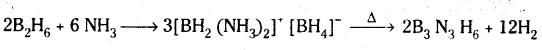
ప్రశ్న 10.
బోరిక్ ఆమ్లం బహ్వణుకగా ఎందుకు ఉంటుంది ?
జవాబు:
బోరిక్ ఆమ్లం పొరలవంటి జాలక నిర్మాణాన్ని కలిగి ఉంటుంది. ఈ నిర్మాణంలో BO3 యూనిట్లు హైడ్రోజన్ బంధాలతో కలుపబడి బహ్వణుక (పాలిమర్) అణువుగా ఏర్పడుతుంది.
ప్రశ్న 11.
డైబోరేన్, బోరజీన్లలో బోరాన్ సంకరకరణం ఏమిటి ?
జవాబు:
- డై బోరేన్లో బోరాన్ sp3 సంకరీకరణం జరుపుకుంటుంది.
- బోరజీన్లో బోరాన్ sp2 సంకరీకరణం జరుపుకుంటుంది.
ప్రశ్న 12.
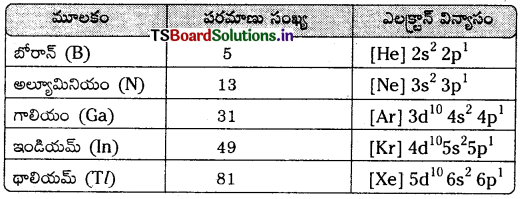
13 గ్రూప్ మూలకాల ఎలక్ట్రాన్ విన్యాసాన్ని రాయండి.
జవాబు:
13 గ్రూపు మూలకాల ఎలక్ట్రాన్ విన్యాసం
ప్రశ్న 13.
బోరజీన్ సాంకేతికాన్ని రాయండి. దాని సాధారణ నామం ఏమిటి?
జవాబు:
- బోరజీనన్ను B3N3H6 అనే ఫార్ములాతో సూచిస్తారు.
- దీని నిర్మాణం బెంజీన్ నిర్మాణాన్ని పోలి ఉండటం వలన దీనిని ఇనార్గానిక్ బెంజీన్ అని అంటారు.
ప్రశ్న 14.
(a) బోరాక్స్
(b) కోలిమనైట్ సాంకేతికాలు ఇవ్వండి.
జవాబు:
a) బోరాక్స్ ఫార్ములా Na2B4O7. 10H2O
b) కోలిమనైట్ ఫార్ములా Ca2B6O11 . 5H2O
ప్రశ్న 15.
అల్యూమినియం ఉపయోగాలు రెండు రాయండి.
జవాబు:
- అల్యూమినియమ్న మిశ్రమ లోహాల తయారీలో ఉపయోగిస్తారు.
- విమాన విడిభాగాల తయారీలో ఉపయోగిస్తారు.
- పైపులు, ట్యూబులు, రాడ్లు, తీగలు వంటి వాటి తయారీలో ఉపయోగిస్తారు.
- నిర్మాణాలలో, రవాణా పరిశ్రమల్లో కూడా దీనిని ఉపయోగిస్తారు.
ప్రశ్న 16.
కింది చర్యల్లో ఏమి జరుగుతుంది ?
(a) LiAlH4, BCl3 మిశ్రమాన్ని అనార్ద్ర ఈథర్లో వెచ్చబెట్టినప్పుడు
b) బోరాక్స్న H2SO4 తో వేడిచేసినప్పుడు
జవాబు:
a) LiAlH4, BCl3 మిశ్రమాన్ని అనార్ద్ర ఈథర్ వెచ్చబెట్టినపుడు డైబోరేన్ ఏర్పడుతుంది.
![]()
b) బోరాక్స్ను H2SO4 తో వేడిచేసినపుడు బోరిక్ ఆమ్లం ఏర్పడును.
Na2B4O7 + H2SO4 + 5H2O → Na2SO4 + 4H3BO3
ప్రశ్న 17.
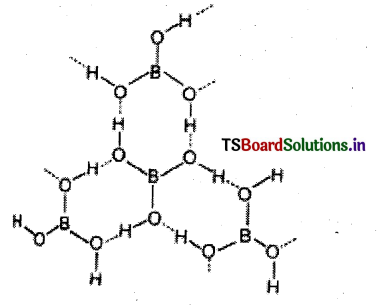
ఆర్థోబోరిక్ ఆమ్ల నిర్మాణాన్ని గీయండి.
జవాబు:
ఆర్థోబోరిక్ ఆమ్లం నిర్మాణం :
![]()
ప్రశ్న 18.
AlCl3 ద్విఅణుక నిర్మాణాన్ని రాయండి.
జవాబు:
AlCl3 ద్విఅణుక నిర్మాణం :
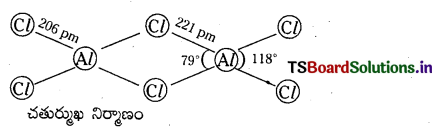
ప్రశ్న 19.
లోహ బోరైడ్లను (10B) రక్షణ కవచాలుగా వాడతారు. ఎందుకు ?
జవాబు:
లోహ బోరైడ్లకు (10B) న్యూట్రాన్లను శోషించుకొనే సామర్థ్యం కలదు. కావున వీనిని న్యూక్లియర్ పరిశ్రమలలో రక్షణ కవచాలుగా వాడతారు.
లఘు సమాధాన ప్రశ్నలు
ప్రశ్న 20.
అల్యూమినియంకు ద్విస్వభావికం ఉన్నదని రుజువు చేసే చర్యలు రాయండి.
జవాబు:
అల్యూమినియం ఆమ్ల మరియు క్షారద్రావణాలలో కరుగుతుంది. కావున దీనికి ద్విస్వభావికం కలదు.
- విలీన ఆమ్లాలలో Al కరిగి H2 వాయువును విడుదల చేస్తుంది.
2 Al + 6 HCl → 2 AlCl3 + 3H2↑ - క్షారాలలో Al కరిగి H2 వాయువును విడుదలచేస్తుంది.
2 Al + 2NaOH + 6H2O → 2 Na+ [Al (OH)4]– + 3H2
ప్రశ్న 21.
ఎలక్ట్రాన్ కొరత గల సమ్మేళనాలంటే ఏమిటి ? BCl3 ఎలక్ట్రాన్ కొరత గల సమ్మేళనమా ? వివరించండి.
జవాబు:
- అష్టక విన్యాసాన్ని పొందని కేంద్రక పరమాణువులు కలిగి ఉన్న అణువులను ఎలక్ట్రాన్ కొరత గల అణువులు అంటారు.
- BCl3 ఎలక్ట్రాన్ కొరత గల సమ్మేళనం. దీనిలో కేంద్రకం B చుట్టూ 6 ఎలక్ట్రాన్లు మాత్రమే ఉంటాయి.
- BCl3 అణువులోని కేంద్రక బోరాన్ పరమాణువు అష్టక విన్యాసాన్ని పొందలేదు.
ప్రశ్న 22.
BF3, B\(F_4^{-}\) లో B – F బంధ దూరాలు వరసగా 130 pm, 143 pm ఎందుకు వేరువేరుగా ఉన్నాయో కారణాలు సూచించండి.
జవాబు:
BF3 లో B పరమాణువు sp2 సంకరీకరణం జరుపుకుంటుంది. ఇది సమతల త్రిభుజాకృతిని కలిగి ఉంటుంది. BF3 లో బోరాన్ పరమాణువు ఫ్లోరిన్ నుంచి ఒక ఎలక్ట్రాన్ జంటను స్వీకరించి దానితో బాక్ బంధంలో పాల్గొంటుంది. కావున B – F బంధము కొంత ద్విబంధ స్వభావాన్ని కలిగి ఉంటుంది.
కాని B\(F_4^{-}\) లో B పరమాణువు sp3 సంకరీకరణం జరుపుకుంటుంది. ఇది టెట్రెహెడ్రల్ ఆకృతిని కలిగి ఉంటుంది. బోరాన్కు ఫ్లోరిన్కు మధ్య బాక్ బంధం ఉండదు.
కావున BF3 లో బంధ దూరం 130PPM ఉంటే B\(F_4^{-}\) లో 143 PPM ఉంటుంది.
ప్రశ్న 23.
B – Cl బంధానికి బంధ భ్రామకం ఉంది కాని BCl3 అణువుకు ద్విధ్రువ భ్రామకం సున్నా ఉంటుంది. వివరించండి.
జవాబు:
B – Cl బంధం దృవణ బంధం కావున బంధ భ్రామకం ఉంటుంది. కాని BCl3 అణువు సౌష్టవ నిర్మాణాన్ని కలిగి ఉంటుంది. మూడు B – Cl బంధ బ్రామకాలు వ్యతిరేక దిశలలో పనిచేయటం వలన మొత్తం ద్విద్రువ భ్రామకం సున్నాగా ఉంటుంది.
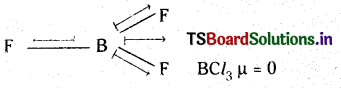
![]()
ప్రశ్న 24.
బోరిక్ ఆమ్లం నిర్మాణాన్ని వివరించండి.
జవాబు:
- బోరిక్ ఆమ్లం పొరలవంటి జాలక నిర్మాణాన్ని కలిగి ఉంటుంది.
- ఈ నిర్మాణంలో BO3 యూనిట్లు హైడ్రోజన్ బంధాలతో కలపబడి ఉంటాయి.
- కావున బోరిక్ ఆమ్లం బాహ్వణుక అణువుగా ఉంటుంది.
ఆర్థోబోరిక్ ఆమ్లం నిర్మాణం :
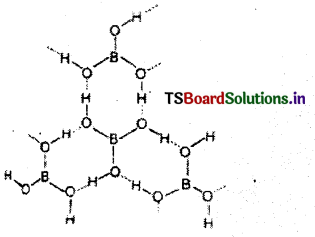
ప్రశ్న 25.
ఏమి జరుగుతుంది :
a) బోరాక్స్న ప్రబలంగా వేడిచేస్తే,
b) బోరిక్ ఆమ్లాన్ని నీటికి కలిపితే,
c) అల్యూమినియాన్ని సజల NaOH తో వేడిచేస్తే
d) అమ్మోనియాతో BF3 చర్య జరిపినప్పుడు
e) అర్థ అల్యూమినాను సజల NaOH ద్రావణంతో చర్య జరిపినప్పుడు
జవాబు:
a) బోరాక్స్న ప్రబలంగా వేడిచేస్తే చివరగా గాజువంటి పదార్థం ఏర్పడుతుంది.
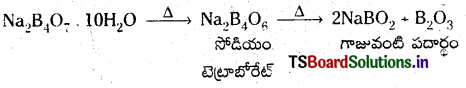
b) బోరిక్ ఆమ్లంనకు నీటిని కలిపితే బోరిక్ ఆమ్లం నీటి నుంచి OH అయాన్లను స్వీకరిస్తుంది.
B(OH)3 + 2H2O → [B(OH)4]– + H3O+
c) Al ను సజల NaOH తో వేడిచేస్తే సోడియం మెటా అల్యూమినేట్తో పాటు H2 వాయువు విడుదలవుతుంది.
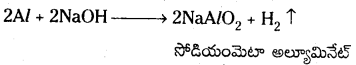
d) BF3, ని NH3 లో చర్య జరిపినపుడు NH3 ఎలక్ట్రాన్ జంటను BF3 కి దానం చేస్తుంది. రెండింటి మధ్య సమన్వయ సమయోజనీయ బంధం ఏర్పడుతుంది.
BF3 + NH3 → [BF3 ← NH3] లేదా [BF3 . NH3]
e) ఆర్ద్ర అల్యూమినాను సజల NaOH ద్రావణంతో చర్య జరిపితే సోడియం మెటా అల్యూమినేట్ ఏర్పడుతుంది.
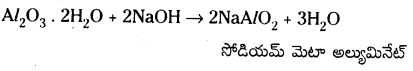
ప్రశ్న 26.
కారణాలు తెలపండి :
సోడియమ్ మెటా అల్యుమినేట్
a) అల్యూమినియం పాత్రలలో గాఢ HNO3 రవాణా చేయవచ్చు.
b) సజల NaOH, అల్యూమినియం ముక్కల మిశ్రమాన్ని మురుగు కాలువను తెరవడానికి వాడతారు.
c) అల్యూమినియం మిశ్రమలోహాన్ని విమానాలను తయారుచేయడానికి వాడతారు.
d) అల్యూమినియం పాత్రలను రాత్రంతా నీళ్ళలో పెట్టకూడదు.
e) అల్యూమినియం తీగలను ప్రసార కేబుల్ తయారీకి వాడతారు.
జవాబు:
a) Al మరియు గాఢ HNO3 కి మధ్య చర్యారాహిత్యం కలదు. అందువలన అల్యూమినియం పాత్రలలో గాఢ HNO3ని రవాణా చేయవచ్చు.
b) సజల NaOH అల్యూమినియమ్ చర్య జరిపి H2 వాయువును విడుదలచేస్తుంది. ఈ వాయు పీడనం వలన మురుగు కాలువలు తెరచుకుంటాయి. కావున సజల NaOH, Al మిశ్రమాన్ని మురుగు కాలువను తెరవటానికి వాడతారు.
c) Al తేలికయిన, బలమైన లోహం. గాలిలో క్షయం చెందదు. కావున దీనిని విమాన విడిభాగాలను తయారుచేయటానికి వాడతారు.
d) అల్యూమినియమ్ పాత్రలను రాత్రంతా నీటిలో పెట్టకూడదు. నీటిలోని లవణాలు పాత్ర ఉపరితలంపై ఉన్న ఆక్సైడ్ పొరతో చర్య జరిపి అల్యూమినియమ్ యొక్క చర్యాశీలతను పెంచుతాయి. దీనివలన Al నీటితో చర్య జరుపుతుంది.
e) అల్యూమినియమ్ తీగలను ప్రసార కేబుల్ తయారీకి వాడతారు. దీనికి కారణం దాని యొక్క మంచి విద్యుద్వాహకత.
ప్రశ్న 27.
Ga, ln, Tl లలో రుణవిద్యుదాత్మకత భేదం ఎందుకు ఎక్కువగా మారదో వివరించండి.
జవాబు:
Ga మరియు ln లలో d ఎలక్ట్రాన్ల వలన పరిరక్షక ప్రభావం తక్కువగా ఉంటుంది. అలాగే Tl లో ‘d’ మరియు ‘f’ ఎలక్ట్రాన్ల వలన పరిరక్షక ప్రభావం తక్కువగా ఉంటుంది. కావున Ga, ln, Tl ల యొక్క పరమాణు పరిమాణంలో పెద్దగా మార్పు ఉండదు. కాని కేంద్రక ఆవేశం మాత్రము పెరుగుతుంది. కావున ఈ మూడు మూలకాల ఋణవిద్యుదాత్మకత విలువలలో భేదం ఎక్కువగా మారదు.
ప్రశ్న 28.
సరైన ఉదాహరణతో బోరాక్స్ పూస పరీక్షను వివరించండి. (March 2013)
జవాబు:
బోరాక్సిని వేడిచేస్తే మొదట నీటి అణువులను కోల్పోయి ఉబ్బి పరిమాణంలో పెద్దదవుతుంది. ఇంకా వేడిచేస్తే అది పారదర్శక ద్రవంగా మారి ఘనీభవనం చెంది గాజులాంటి పదార్థంగా మారుతుంది. దీనిలో సోడియం బొరేట్ మరియు B2O3 ఉంటాయి. ఈ B2O3ను లోహ ఆక్సైడ్ తో కలిపి వేడి చేస్తే లోహ మెటాబొరేట్లు ఏర్పడతాయి. ఈ మెటాబొరేట్లు ప్రత్యేకమైన రంగును కలిగి ఉంటాయి. వచ్చిన రంగును బట్టి లవణంలోని కేటయాను గుర్తించవచ్చును.
Na2B4O7 + CoO → 2NaBO2 + Co (BO2)
ఆక్సీకరణ, క్షయకరణ జ్వాలలో వేడి చేసినపుడు ఒక్కొక్క లోహం ఒక్కొక్క రంగుగల మెటాబోరేట్లను ఏర్పరుస్తుంది. దీనిని బోరాన్ పూస పరీక్ష అంటారు.
ప్రశ్న 29.
డైబోరేన్ నిర్మాణాన్ని వివరించండి.
జవాబు:
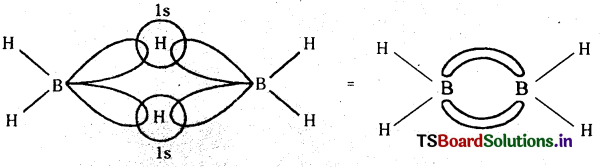
డైబోరేన్ నిర్మాణము :
- డైబోరేన్లో రెండు సమతల BH2 గ్రూపులు ఉంటాయి. ఈ రెండు BH2 గ్రూపులను కలుపుతూ రెండు H పరమాణువులు ఉంటాయి. రెండు బోరాన్ పరమాణువులకు అతకబడి ఉన్న నాలుగు H లను అంత్య హైడ్రోజన్లు అని, BH2 గ్రూపులను కలిపే రెండు H పరమాణువులను వారధి (బ్రిడ్జ్) H పరమాణువులని అంటారు.
- B2H6 లో రెండు బోరాన్ పరమాణువులు sp3 సంకరీకరణం జరుపుకొని నాలుగు sp3 సంకర ఆర్బిటాళ్ళను ఏర్పరుస్తాయి. నాలుగు sp3 సంకర ఆర్బిటాళ్లలో ఒక ఆర్బిటాల్లో ఎలక్ట్రాన్ ఉండదు.
- ప్రతి బోరాన్లోని రెండు బంధ ఎలక్ట్రాన్లు గల sp3 సంకర ఆర్బిటాల్స్లో రెండు హైడ్రోజన్ల యొక్క s ఆర్బిటాల్స్తో అతిపాతం చెంది సహజమైన B-H బంధాలు (2 – కేంద్రక 2 – ఎలక్ట్రాన్లు) ఏర్పడతాయి.
- ఒక బోరాన్లోని బంధ ఎలక్ట్రాన్ గల sp3 సంకర ఆర్బిటాల్, వేరొక బోరాన్లోని ఖాళీ sp3 సంకర ఆర్బిటాల్ మరియు H యొక్క 1s ఆర్బిటాల్తో అతిపాతం చెంది B-H-B (బిడ్జ్ బంధాన్ని ఏర్పరుస్తాయి. ఈ విధంగా B2H6 లో రెండు B-H-B బ్రిడ్జ్ బంధాలు ఏర్పడతాయి. ఈ బంధాలనే బనానా బంధాలు అని లేదా 3-కేంద్రక-2-ఎలక్ట్రాన్ బంధాలని అంటారు.
ప్రశ్న 30.
ఆమ్లాలతో అల్యూమినియం చర్యలను వివరించండి.
జవాబు:
- అల్యూమినియమ్ విలీన లేదా గాఢ HCl లో కరిగి H2 వాయువును విడుదలచేస్తుంది.
2Al + 6HCl → 2AlCl3 + 3H2 ↑ - అల్యూమినియమ్ విలీన H2SO4 లో H2 ను విడుదలచేస్తుంది.
2Al + 3H2SO4 → Al2 (SO4)3 + 3H2 ↑ - అల్యూమినియమ్ గాఢ H2SO4 లో కరిగి SO4 ను ఇస్తుంది.
2Al + 6H2SO4 → Al2(SO4)3 + 3SO2 + 6H2O - అతి విలీన HNO3ని అల్యూమినియమ్ NH4NO3 గా క్షయకరణం చేస్తుంది.
8Al + 30HNO3 → 8Al (NO3)3 + 3NH4NO3 + 9H2O - గాఢ HNO3 తో Al క్రియారహితం అవుతుంది. లోహపు ఉపరితలంపై పలుచని ఆక్సైడ్ పొర ఏర్పడటం వలన క్రియారాహిత్యం వస్తుంది.
![]()
ప్రశ్న 31.
గ్రూపు 13లో బోరాన్ అసంగత ప్రవర్తనను సంక్షిప్తంగా రాయండి.
జవాబు:
బోరాన్ పరమాణు సైజు చిన్నది కావటం, అయొనైజేషన్ పొటెన్షియల్ ఎక్కువగా ఉండటం వలన మిగిలిన మూలకాలతో అసంగత ప్రవర్తనను చూపిస్తుంది. ఉదా :
- బోరాన్ అలోహం, Al ద్వంద్వ స్వభావం గల లోహం Ga, ln, Tl లు లోహాలు.
- బోరాన్ ఎల్లప్పుడు కోవలంట్ సమ్మేళనాలను ఇస్తుంది. కాని మిగిలిన మూలకాలు అయానిక సమ్మేళనాలను ఇస్తాయి.
- బోరాన్కు సిలికాన్తో కర్ణ సంబంధం ఉంటుంది. మిగిలిన మూలకాలు ఈ కర్ణ సంబంధాన్ని చూపవు.
- ఆమ్లాల నుండి బోరాన్ H2 ను స్థానభ్రంశం చేయదు. కాని మిగిలిన మూలకాలు H2 స్థానభ్రంశం చెందిస్తాయి. బోరాన్ ఆక్సైడ్ ఆమ్ల ఆక్సెడ్. కాని మిగిలిన మూలకాల ఆక్సైడ్లు ద్విస్వభావ ఆక్సైడ్లుగా గాని క్షార ఆక్సైడ్లుగా గాని ఉంటాయి.
- సరళ బోరేట్లు, సిలికేటులు తేలికగా పాలిమరీకరణం చెంది పాలీ ఆమ్లాలను ఇస్తాయి. మిగిలిన మూలకాలు పాలిమర్ ఆమ్లాలను ఇవ్వవు.
- బోరాన్ అత్యధిక కో వేలన్సీ 4. ఇతర మూలకాల అత్యధిక కోవలన్సీ 6.
- స్థిరమైన కోవలంట్ హైడ్రేడ్లను ఇస్తుంది. మిగిలిన మూలకాలు స్థిరమైన హైడ్రైడ్లను ఇవ్వవు.
ప్రశ్న 32.
అల్యూమినియం సజల HNO3 తో చర్య జరుపుతుంది కాని గాఢ HNO3 తో చర్య జరపదు. వివరించండి.
జవాబు:
విలీన HNO3 తో అల్యూమినియమ్ చర్యజరిపి HNO3 ని NH4 NO3 గా క్షయకరణం చేస్తుంది.
8Al + 3OHNO3 → 8Al(NO3)3 + 3NH4NO3 + 9H2O
కాని గాఢ HNO3 కి అల్యూమినియమ్ను కలిపినపుడు లోహపు తలంపై పలుచని ఆక్సైడ్పొర ఏర్పడుతుంది.. ఈ. ఆక్సైడ్ పొర రక్షిత పొరగా పనిచేసి Al ని HNO3 తో చర్య జరగకుండా అడ్డుకుంటుంది. కావున గాఢ HNO3 తో Al క్రియారహితం అవుతుంది.
ప్రశ్న 33.
డైబోరేన్ ను తయారుచేసే రెండు పద్ధతులు రాయండి.
జవాబు:
డైబోరేన్ [B2H6] ను తయారుచేయు పద్ధతులు :
బోరాన్ ట్రై ఫ్లోరైడు లిథియమ్ అల్యూమినియమ్ హైడ్రైడ్తో డైఈథైల్ ఈథర్లో చర్య జరిపి డైబోరేన్ను తయారుచేస్తారు.
4BF3 + 3LiAlH4 → 2B2H6 + 3LiF + 3AlF3
- ప్రయోగశాలలో సోడియం బోరోహైడ్రైడు, అయోడిన్ ఆక్సీకరణం చేసి డైబోరేన న్ను తయారుచేస్తారు.
2NaBH4 + I2 → B2H6 + 2Nal + H2 - పారిశ్రామికంగా డైబోరేన్ న్ను ఉత్పత్తి చేయడానికి BF3 ని సోడియం హైడ్రైడ్తో చర్య జరిపిస్తారు.

ప్రశ్న 34.
డైబోరేన్ ఈ కింది వాటితో ఏ విధంగా చర్య జరుపుతుంది ?
a) H2O
b) CO
c) N(CH3)3
జవాబు:
a) డైబోరేన్ నీటితో చర్య : డైబోరేన్ నీటిలో జలవిశ్లేషణ చెంది బోరిక్ ఆమ్లాన్ని ఇస్తుంది.
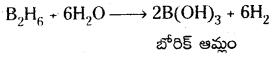
b) డైబోరేన్ CO తో చర్య : డైబోరేన్ 1000°C ఉష్ణోగ్రత మరియు 2 atm పీడనం వద్ద CO తో చర్య జరిపి బోరేన్ కార్బోనైల్ను ఏర్పరుస్తుంది.

c) డైబోరేన్ N(CH3)3 తో చర్య : డైబోరేన్ N(CH3)3 తో చర్య జరిపి బోరాన్ సంకలితాన్ని ఏర్పరుస్తుంది.
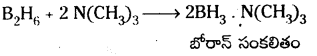
ప్రశ్న 35.
Al2O3 ద్విస్వభావం కలదని సరైన చర్యలతో వివరించండి.
బోరాన్ సంకలితం
జవాబు:
Al2O3 కు ద్విస్వభావం కలదు. ఇది ఆమ్లాలతో మరియు క్షారాలతో చర్య జరిపి లవణాలను ఏర్పరుస్తుంది.
ఆమ్లాలతో చర్య : ‘Al2O3 ఆమ్లాలతో ఈ క్రింది విధంగా చర్య జరుపుతుంది.
Al2O3 +6HCl → 2AlCl3 + H2O
క్షారాలతో చర్య : Al2O3 క్షారాలతో ఈ క్రింది విధంగా చర్య జరుపుతుంది.
Al2O3 + 2NaOH → NaAlO2 + H2O
ప్రశ్న 36.
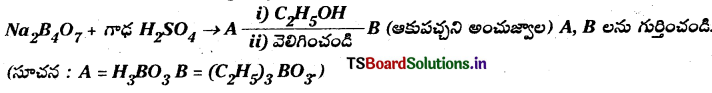
జవాబు:
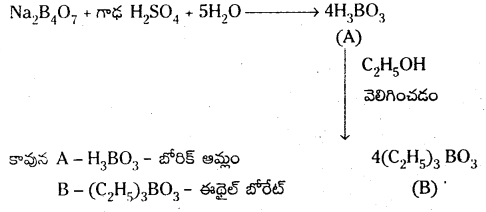
దీర్ఘ సమాధాన ప్రశ్నలు
ప్రశ్న 37.
బోరాక్స్న, బోరిక్ ఆమ్లాన్ని ఎలా తయారుచేస్తారు ? వాటిమీద ఉష్ణం చర్యను వివరించండి.
జవాబు:
బోరాక్స్ తయారీ : బోరిక్ ఆమ్లంను వేడిచేయగా టెట్రాబోరిక్ ఆమ్లం ఏర్పడుతుంది. దీనిని NaOH తో చర్య జరపగా బోరాక్స్ ఏర్పడును.
![]()
బోరాకున్ను అధికంగా వేడిచేస్తే గాజులాంటి పదార్థంగా మారుతుంది. దీనినే బోరాక్స్ పూస అంటారు.
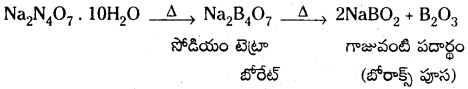
బోరిక్ ఆమ్లం తయారీ : బోరాక్స్ను గాఢ H2SO4 తో చర్య జరిపినపుడు బోరిక్ ఆమ్లం ఏర్పడుతుంది.
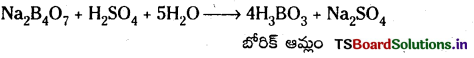
బోరిక్ ఆమ్లంను వేడిచేయగా మెటాబోరికామ్లం ఏర్పడుతుంది. దీనిని ఇంకా వేడిచేస్తే బోరిక్ ఆక్సైడ్ ఏర్పడుతుంది.
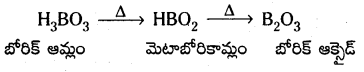
![]()
ప్రశ్న 38.
డైబోరేన్ ను ఎలా తయారుచేస్తారు ? దాని నిర్మాణాన్ని వివరించండి.
జవాబు:
డైబోరేన్ [B2H6] ను తయారుచేయు పద్ధతులు :
- బోరాన్ ట్రై ఫ్లోరైడ్ను లిథియమ్ అల్యూమినియమ్ హైడ్రైడ్తో డైఈథైల్ ఈథర్లో చర్య జరిపి డైబోరేన్ ను తయారుచేస్తారు.
4BF3 + 3LiAlH4 → 2B2H6 + 3LiF + 3AlF3 - ప్రయోగశాలలో సోడియం బోరోహైడ్రైడ్న, అయోడిన్తో ఆక్సీకరణం చేసి డైబోరేన్ తయారుచేస్తారు.
2NaBH4 + I2 → B2H6 + 2Nal + H2
పారిశ్రామికంగా డైబోరేన్ ను ఉత్పత్తి చేయడానికి BF3 ని సోడియం హైడ్రైడ్తో చర్య జరిపిస్తారు.
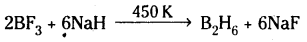
డైబోరేన్ నిర్మాణము :
- డైబోరేన్లో రెండు సమతల BH2 గ్రూపులు ఉంటాయి. ఈ రెండు BH2 గ్రూపులను కలుపుతూ రెండు H పరమాణువులు ఉంటాయి. రెండు బోరాన్ పరమాణువులకు అతకబడి ఉన్న నాలుగు H లను అంత్య హైడ్రోజన్లు అని, BH2 గ్రూపులను కలిపే రెండు H పరమాణువులను వారధి (బ్రిడ్జ్) H పరమాణువులని అంటారు.
- B2H6 లో రెండు బోరాన్ పరమాణువులు sp3 సంకరీకరణం జరుపుకొని నాలుగు sp3 సంకర ఆర్బిటాళ్ళను ఏర్పరుస్తాయి. నాలుగు sp3 సంకర ఆర్బిటాళ్లలో ఒక ఆర్బిటాల్లో ఎలక్ట్రాన్ ఉండదు.
- ప్రతి బోరాన్లోని రెండు బంధ. ఎలక్ట్రాన్లు గల sp3 సంకర ఆర్బిటాల్స్తో రెండు హైడ్రోజన్ల యొక్క s – ఆర్బిటాల్స్తో అతిపాతం చెంది సహజమైన B – H బంధాలు (2 – కేంద్రక 2 – ఎలక్ట్రాన్లు) ఏర్పడతాయి.
- ఒక బోరాన్లోని బంధ ఎలక్ట్రాన్ గల sp3 సంకర ఆర్బిటాల్, వేరొక బోరాన్లోని ఖాళీ sp3 సంకర ఆర్బిటాల్ మరియు H యొక్క 1s ఆర్బిటాల్తో అతిపాతం చెంది B-H-B బ్రిడ్జ్ బంధాన్ని ఏర్పరుస్తాయి. ఈ విధంగా B2H6 లో రెండు B-H-B బ్రిడ్జ్ బంధాలు ఏర్పడతాయి. ఈ బంధాలనే బనానా బంధాలు అని లేదా 3-కేంద్రక-2-ఎలక్ట్రాన్ బంధాలని అంటారు.
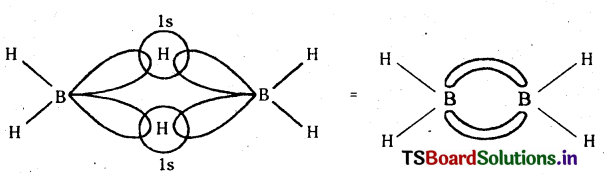
ప్రశ్న 39.
డైబోరేన్ను తయారుచేసే ఏవైనా రెండు పద్ధతులు రాయండి. అది ఈ కింది వాటితో ఏ విధంగా చర్య జరుపుతుంది?
a) కార్బన్ మోనాక్సైడ్
b) అమ్మోనియా
జవాబు:
డైబోరేన్ [B2H6] ను తయారుచేయు పద్ధతులు :
- బోరాన్ ట్రై ఫ్లోరైడ్ను లిథియమ్ అల్యూమినియమ్ హైడ్రైడ్ డైఈథైల్ ఈథర్లో చర్య జరిపి డైబోరేన్ను తయారుచేస్తారు.
4BF3 + 3LiAlH4 → 2B2H6 + 3LiF + 3AlF3 - ప్రయోగశాలలో సోడియం బోరోహైడ్రైడ్న, అయోడిన్తో ఆక్సీకరణం చేసి డైబోరేన్ ను తయారుచేస్తారు.
2NaBH4 + I2 → B2HË6 + 2Nal + H2 - పారిశ్రామికంగా డైబోరేన్ను ఉత్పత్తి చేయడానికి BF3 ని సోడియం హైడ్రైడ్తో చర్య జరిపిస్తారు.
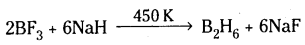
a) డైబోరేన్ కార్బన్ మోనాక్సైడ్తో చర్య : డైబోరేన్ 1000°C ఉష్ణోగ్రత మరియు 22atm పీడనం వద్ద CO తో చర్య జరిపి బోరేన్ కార్బనైల్ అనే బోరాన్ సంకలితాన్ని ఏర్పరుస్తుంది.
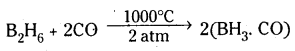
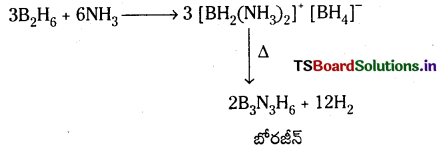
b) డైబోరేన్ అమ్మోనియాతో చర్య డైబోరేన్ అమ్మోనియాతో చర్యనొంది మొదట B6H6. 2NH3 ని ఇస్తుంది. దీనినే
(BH2(NH3)2)+ B\(\mathrm{H}_4^{-}\) గా కూడా వ్రాయవచ్చు. దీనిని ఇంకా వేడిచేస్తే బోరజీన్ ఏర్పడుతుంది. బోరజీన్కు బెంజీన్ వంటి వలయ నిర్మాణం ఉంటుంది. కావున దీనిని ఇనార్గానిక్ బెంజీన్ అని కూడా అంటారు.