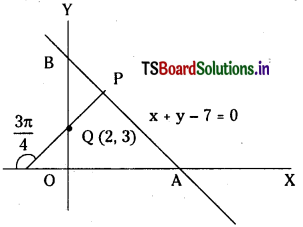
Telangana TSBIE TS Inter 1st Year Chemistry Study Material 2nd Lesson మూలకాల వర్గీకరణ – ఆవర్తన ధర్మాలు Textbook Questions and Answers.
TS Inter 1st Year Chemistry Study Material 2nd Lesson మూలకాల వర్గీకరణ – ఆవర్తన ధర్మాలు
అత్యంత లఘు సమాధాన ప్రశ్నలు
ప్రశ్న 1.
మెండలీవ్ ఆవర్తన నియమ పద్ధతికి, ఆధునిక ఆవర్తన నియమ పద్ధతికి గల తేడా ఏమిటి ?
జవాబు:
మెండలీవ్ ఆవర్తన నియమము పరమాణు భారాలపై ఆధారపడి ఉండును. ఆధునిక ఆవర్తన నియమము ఎలక్ట్రాన్ విన్యాసంపై ఆధారపడినది.
మెండలీవ్ ఆవర్తన నియమము : మూలకాల భౌతిక రసాయనిక ధర్మాలు, వాటి పరమాణు భారాల ఆవర్తన ప్రమేయాలు.
ఆధునిక ఆవర్తన నియమము : మూలకాల భౌతికరసాయన ధర్మాలు, వాటి ఎలక్ట్రాన్ విన్యాసాల ఆవర్తన ప్రమేయాలు.
ప్రశ్న 2.
Z = 114 గల మూలకాన్ని ఏ పీరియడ్, ఏ గ్రూప్లో ఉంచుతారు ?
జవాబు:
Z = 114 మూలకము యొక్క బాహ్య ఎలక్ట్రాన్ విన్యాసము 7s2 7p3. ఈ మూలకం బాహ్య కర్పర ప్రధాన క్వాంటం సంఖ్య 7 కనుక అది ఏడవ పీరియడ్కు చెందుతుంది. బాహ్య కర్పరంలోని ఎలక్ట్రాన్ల సంఖ్య 4 కనుక గ్రూపు సంఖ్య 4. Z-114 మూలకం ఏడవ పీరియడ్ మరియు నాలుగవ గ్రూపులో ఉంటుంది.
![]()
ప్రశ్న 3.
ఆవర్తన పట్టికలో మూడో పీరియడ్, పదిహేడో గ్రూప్ లో ఉన్న మూలకం పరమాణు సంఖ్యను తెలపండి.
జవాబు:
17వ గ్రూపులోని మూలకము హాలోజన్. మూడవ పీరియడ్లోని హాలోజన్ మూలకము క్లోరిన్. క్లోరిన్ పరమాణు సంఖ్య పదిహేడు (17).
ప్రశ్న 4.
a) లారెన్స్ బర్క్లీ ప్రయోగశాల
b) సీబర్గ్ గ్రూప్
వీరిచే నామకరణం చేయబడిన మూలకాలు ఏవై ఉంటాయి ?
జవాబు:
పరమాణు సంఖ్య 97 మరియు 98 గల మూలకాలు Berkeley లో గల కాలిఫోర్నియా యూనివర్శిటీలో కనుక్కోబడ్డాయి. వాటికి Berkelium (97) మరియు కాలిఫోర్నియం (98) గా నామకరణం చేసారు.
ప్రశ్న 5.
ఒకే గ్రూప్ లోని మూలకాలు సారూప్య భౌతిక, రసాయన ధర్మాలను ఎట్లా కలిగి ఉంటాయి ?
జవాబు:
ఒకే గ్రూపులోని మూలకాలు ఒకే విధమైన బాహ్య ఎలక్ట్రాన్ విన్యాసాన్ని కలిగి ఉండుట వలన సారూప్య భౌతిక రసాయన ధర్మాలను కలిగి ఉంటాయి.
ప్రశ్న 6.
ప్రాతినిధ్య మూలకాలంటే ఏమిటి ? వాటి వేలన్సీ కక్ష్య విన్యాసాన్ని తెలపండి.
జవాబు:
” జడవాయువులు మినహా మిగిలిన s మరియు p బ్లాకు మూలకాలను ప్రాతినిధ్య మూలకాలంటారు. వాటి బాహ్య స్థాయి విన్యాసం ns1-2 np0-5
ప్రశ్న 7.
ఆవర్తన పట్టికలో f – బ్లాక్ మూలకాల స్థానాన్ని సమర్థించండి.
జవాబు:
- f – బ్లాకు మూలకాలు రెండు శ్రేణులుగా ఉన్నాయి. అవి 4f శ్రేణి మరియు 5f శ్రేణి.
- అవి ఒకే విధమైన సాధారణ ఎలక్ట్రాన్ విన్యాసాన్ని కలిగి ఉన్నాయి. (n – 2) f1 – 14 (n – 1) d0 – 1 ns2
- 4f శ్రేణి మూలకాలు ఒకే విధమైన ధర్మాలు కలిగి ఉన్నాయి. అదే విధంగా 5f శ్రేణి మూలకాలు ఒకే విధమైన ధర్మాలు కలిగి ఉన్నాయి.
- సారూప్య ధర్మాలు గల మూలకాలను ఒకే నిలువు పట్టీలో ఉంచాలనే వర్గీకరణ సూత్రం అమలు అయ్యేటట్లు ఆవర్తన పట్టిక నిర్మాణాన్ని చేయడానికి 4f. 5f – అంతర పరివర్తన శ్రేణుల మూలకాలను ఆవర్తన పట్టికలో వేరుగా ఉంచారు.
ప్రశ్న 8.
‘z’ అనే మూలకం పరమాణు సంఖ్య 34. ఆవర్తన పట్టికలో దాని స్థానాన్ని తెలపండి.
జవాబు:
z = 34 ఎలక్ట్రాన్ విన్యాసం
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4
బాహ్యకర్పర ప్రధాన క్వాంటం సంఖ్య పీరియడ్ను, దానిలోని ఎలక్ట్రాన్ల సంఖ్య గ్రూపును తెలియచేస్తాయి. అందువల్ల z = 34 మూలకం 4వ పీరియడ్ మరియు 6వ గ్రూపుకు చెందినది.
ప్రశ్న 9.
పరివర్తన మూలకాల అభిలాక్షణిక ధర్మాలకు కారణమయ్యే అంశాలు ఏవి ?
జవాబు:
- అల్ప పరమాణు పరిమాణం
- అధిక కేంద్రక ఆవేశం
- అనేక ఆక్సీకరణ స్థితులు (చర సంయోజకత)
- ‘d’ ఆర్బీటాళ్లు బంధాలు ఏర్పరచుటకు అందుబాటులో ఉండుట.
ఈ కారణాలవల్ల పరివర్తన మూలకాలు అభిలాక్షణికమైన ధర్మాలను ప్రదర్శిస్తాయి.
ప్రశ్న 10.
d – బ్లాక్, f – బ్లాక్ మూలకాల బాహ్య కక్ష్యల ఎలక్ట్రాన్ విన్యాసాన్ని ఇవ్వండి.
జవాబు:
d బ్లాకు మూలకాల సాధారణ ఎలక్ట్రాన్ విన్యాసం (n – 1) d1 – 10 ns1 or 2
f బ్లాకు మూలకాల విన్యాసం (n – 2) f1 – 14 (n – 1)d0 or 1 ns2
![]()
ప్రశ్న 11.
డొబరైనర్ త్రిక నియమాన్ని, న్యూలాండ్ అష్టక నియమాన్ని నిర్వచించి ఒక్కొక్క ఉదాహరణను ఇవ్వండి.
జవాబు:
డొబరైనర్ త్రికాలు : పరమాణు భారాల ఆరోహణ క్రమంలో అమర్చబడి ధర్మాలలో పోలికలు గల మూడు మూలకాల సమూహాలను త్రికాలు అంటారు.
మూడు మూలకాలను వాటి పరమాణు భారాల ఆరోహణ క్రమంలో అమరిస్తే, మధ్యమూలకం పరమాణు భారం మిగిలిన రెండు మూలకాల పరమాణు భారాల సరాసరి విలువకు సమానం. దీనినే త్రిక సిద్ధాంతం అంటారు.
ఉదా :

న్యూలాండ్స్ అష్టక నియమం : మూలకాలను వాటి పరమాణు భారాలు పెరిగే క్రమంలో అమరిస్తే, ప్రతి ఎనిమిదవ మూలకం మొదటి మూలకాన్ని దాని ధర్మాలతో పోలి వుంటుంది. ఈ సంబంధం సంగీత స్వరాలలో ఎనిమిదో స్వరం మొదటి స్వరాన్ని పోలినట్లుంటుంది.

ప్రశ్న 12.
మెండలీవ్ ఆవర్తన పట్టికలోని అసంగత మూలకాల జంటలు ఏవి ?
జవాబు:
మెండలీవ్ ఆవర్తన పట్టికలో మూలకాలను పరమాణు భారాలు పెరిగే క్రమంలో అమర్చడం జరిగింది. పరమాణు భారక్రమాన్ని ఖచ్చితంగా పాటిస్తే కొన్ని మూలకాలు వర్గీకరణ క్రమంలో ఇమడటంలేదు. అందువల్ల కొన్ని జతల మూలకాలలో పరమాణు భారాల వరుసలు అపక్రమంలో ఉన్నాయి. వీటినే అసంగత మూలకాల జంటలు అంటారు.
- ఆర్గాన్ – పొటాషియం
- కోబాల్ట్ – నికెల్
- టెల్యూరియం – అయోడిన్
- థోరియం – ప్రోటాక్టినియంలు
కాని ఇవి మాత్రం పరమాణు సంఖ్యల ఆరోహణ క్రమంలోనే ఉన్నాయి.
ప్రశ్న 13.
పీరియడ్లో, గ్రూప్లో పరమాణు వ్యాసార్థం ఎలా మార్పు చెందుతుంది ? మార్పును ఎట్లా విశదీకరిస్తారు ?
జవాబు:
పరమాణు వ్యాసార్ధం : ఒక గ్రూపులో పై నుండి క్రిందికి వచ్చిన కొద్దీ పరమాణు వ్యాసార్ధం పెరుగుతుంటుంది. కారణం గ్రూపులో కిందికి వచ్చిన కొద్దీ వేలన్సీ ఎలక్ట్రాన్లు కొత్త కక్ష్యలో ప్రవేశిస్తాయి. కేంద్రక ఆవేశం పెరిగినా కూడా వేలన్సీ ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ అధికంగా ఉండనందున కక్ష్యలు దూరంగా జరుగుతాయి. అప్పుడు పరమాణు సైజు పెరుగుతుంది.
ఒక పీరియడ్లో ఎడమ నుండి కుడికి వెళ్ళిన కొద్దీ పరమాణు సైజు తగ్గుతుంది. కారణం భేదాత్మక ఎలక్ట్రాన్ అదే కక్ష్యలోకి ప్రవేశిస్తుంది. కేంద్రక ఆవేశం కూడా పెరగడం వల్ల ఈ కక్ష్యపై కేంద్రక ఆకర్షణ పెరుగుతుంది. దాని వల్ల కక్ష్యల సైజు తగ్గి పరమాణు సైజు, తగ్గుతుంది.
ప్రశ్న 14.
N-3, O-2, F–, Na+, Mg+2 Al+3 లను పరిశీలించండి.
a) వీటిలో గల సారూప్యత ఏమిటి ?
b) వీటిని అయానిక వ్యాసార్థ పెరుగుదల క్రమంలో అమర్చండి.
జవాబు:
N-3, O-2, F–, Na+, Mg+2, Al+3 అయానులు సమాన సంఖ్యలో ఎలక్ట్రాన్లను కలిగి ఉన్నాయి. వీటిని సమ ఎలక్ట్రాన్ శ్రేణి అంటారు. సమ ఎలక్ట్రాన్ శ్రేణిలో అయానులు పరమాణు సంఖ్య పెరిగే క్రమంలో అమరిస్తే అయానిక వ్యాసార్ధం క్రమంగా తగ్గుతుంది. అందువల్ల పరమాణు సంఖ్య ఎక్కువగాఉన్న అయాను చిన్నదిగా ఉంటుంది.
Al+3 < Mg2 < Na+ < F– < O-2 < N-3
ప్రశ్న 15.
అయొనైజేషన్ ఎంథాల్పీని నిర్వచించినప్పుడు, భూస్థితిలోని ఒంటరి పరమాణువు అను పదానికి గల ప్రాముఖ్యం ఏమిటి? (సూచన : పోల్చడానికి అవసరమైంది.)
జవాబు:
వివిధ మూలకాల అయొనైజేషన్ ఎంథాల్పీలను పోల్చడానికి ఎంథాల్పీలను సారూప్య పరిస్థితులలో కొలవాలి. అందువల్లనే వాయుస్థితిలోని ఒంటరి తటస్థ పరమాణువును ప్రామాణికంగా తీసుకోవడం జరిగింది.
ప్రశ్న 16.
భూస్థితిలో హైడ్రోజన్ పరమాణువులోని ఎలక్ట్రాన్ శక్తి -2.18 × 10-18J. హైడ్రోజన్ పరమాణువు అయొనైజేషన్ ఎంథాల్పీని J mol-1 లలో లెక్కకట్టండి.
జవాబు:
హైడ్రోజన్ పరమాణువులోని ఎలక్ట్రాన్ భూస్థితిలో ప్రథమశక్తిస్థాయిలో ఉంటుంది. పరమాణు హైడ్రోజన్ యొక్క అయొనైజేషన్ ఎంథాల్పీని లెక్కించడానికి దానిలోని ఎలక్ట్రానన్ను పరమాణువునుంచి వేర్పరచాలి. అప్పుడు దాని శక్తి OJ
అయొనైజేషన్ ఎంథాల్పీ = Eoo – E1 = 0 – (-2.18 × 10-18) = 2.18 × 10-18 J
అయొనైజేషన్ ఒక మోల్కు దీని విలువ = 2.18 × 10-18 × 6.023 × 1023 J/mole = 1312 KJ / mole
ప్రశ్న 17.
‘O’ అయొనైజేషన్ ఎంథాల్పీ ‘N’ కంటే తక్కువ – విశదీకరించండి.
జవాబు:
నైట్రోజన్ ఎలక్ట్రాన్ విన్యాసం 1s2 2s2 \(2 p_x^1 2 p_y^1 2 p_z^1\). ఈ ఎలక్ట్రాన్ విన్యాసం సగం నిండిన ఆర్బిటాళ్ళను కలిగి ఉంది అందువల్ల స్థిరమైనది. ఆక్సిజన్ 1s2 2s2 \(2 p_x^2 2 p_y^1 2 p_z^1\) జతకూడిన 2p ఎలక్ట్రాన్ల మధ్య వికర్షణ ఫలితంగా అయొనైజేషన్ ఎంథాల్పీ తగ్గుతుంది.
అందువల్ల I.P (O2) < I.P (N2)
ప్రశ్న 18.
కింది ప్రతి జంటలో దేనికి అధిక రుణాత్మక ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఉంది ?
a) O or F
b) For Cl
జవాబు:
a) ఒక పీరియడ్లో ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ పెరుగుతుంది. అందువల్ల ఫ్లోరిన్క ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఎక్కువ.
b) For Cl
ఫ్లోరిన్కు గల స్వల్ప పరిమాణం కారణంగా దానిలో ఎలక్ట్రాన్ సాంద్రత ఎక్కువ. అందువల్ల కొత్తగా చేరే ఎలక్ట్రాన్ వికర్షించబడుతుంది. ఈ కారణంగా ‘ఫ్లోరిన్’ కు ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ తక్కువ. కనుక ‘క్లోరిన్క’ ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఎక్కువ.
ప్రశ్న 19.
లోహాలకు, అలోహాలకు ఉన్న ముఖ్యమైన తేడాలు ఏవి ?
జవాబు:
లోహాలు గది ఉష్ణోగ్రత వద్ద ఘనపదార్థాలు. వాటికి ద్రవీభవన, బాష్పీభవన ఉష్ణోగ్రతలు అధికంగా ఉంటాయి. అవి ఉత్తమ విద్యుత్ మరియు ఉష్ణ వాహకాలు. రసాయనికంగా లోహాలు అధిక ధన విద్యుదాత్మకతను కలిగి ఉంటాయి.
అలోహాలు ఘనపదార్థాలుగా గాని, వాయుస్థితిలోగాని ఉంటాయి. అలోహాలకు ద్రవీభవన, బాష్పీభవన ఉష్ణోగ్రతలు తక్కువగా ఉంటాయి. అలోహాలు అథమ ఉష్ణ మరియు అథమ విద్యుత్ వాహకాలు. అలోహాలలో ఋణ విద్యుదాత్మక విలువలు ఎక్కువగా ఉంటాయి.
ప్రశ్న 20.
ఆవర్తన పట్టిక సహాయంతో కింది మూలకాలను గుర్తించండి.
a) బాహ్య ఉపస్థాయిలో 5 ఎలక్ట్రాన్లు ఉన్నాయి.
b) రెండు ఎలక్ట్రాన్లను పోగొట్టుకోగలది
c) రెండు ఎలక్ట్రాన్లను గ్రహించగలది.
జవాబు:
a) బాహ్యశక్తి స్థాయిలోని ఎలక్ట్రాన్ల సంఖ్య ఆవర్తన పట్టికలో గ్రూప్ సంఖ్యకు సమానం. బాహ్య ఉపస్థాయిలో 5 ఎలక్ట్రాన్లు ఉన్నాయి కాబట్టి బాహ్య శక్తి స్థాయిలోని ఎలక్ట్రాన్ల సంఖ్య 7. అంటే s ఉపస్థాయిలో 2 ఎలక్ట్రాన్లు p ఉపస్థాయిలో 5 ఎలక్ట్రాన్లు ఉంటాయి. కనుక బాహ్యస్థాయిలో 7 ఎలక్ట్రాన్లు ఉంటాయి. కనుక మూలకం 7వ గ్రూపుకి చెందినది.
b) 2 ఎలక్ట్రాన్లను పోగొట్టుకోగలిగిన మూలకము బాహ్యస్థాయిలో 2 ఎలక్ట్రాన్లు ఉంటాయి. కనుక ఆ మూలకం 2వ గ్రూపుకు చెందినది.
c) ప్రతీ మూలక పరమాణువు బాహ్యస్థాయిలో ఎలక్ట్రాన్ అష్టకాన్ని పొందడానికి వీలుగా ఎలక్ట్రాన్లను గ్రహించుట లేదా కోల్పోవుట చేస్తుంది. రెండు ఎలక్ట్రాన్లను గ్రహించే మూలకం బాహ్యస్థాయిలో ఆరు ఎలక్ట్రాన్లను కలిగి ఉంటుంది. కనుక మూలకం ఆరవ గ్రూపుకి చెందినది.
ప్రశ్న 21.
s, p, d, f బ్లాక్ మూలకాల బాహ్య ఎలక్ట్రాన్ విన్యాసాన్ని ఇవ్వండి.
జవాబు:
S – బ్లాక్ మూలకాలు బాహ్య ఎలక్ట్రాన్ విన్యాసం ns1 లేదా ns2
p – బ్లాక్ మూలకాల బాహ్య ఎలక్ట్రాన్ విన్యాసం ns2 np1 నుంచి ns2 np6
d – బ్లాక్ మూలకాల బాహ్య ఎలక్ట్రాన్ విన్యాసం (n – 1) d1 – 10 ns1 లేదా 2
f – బ్లాక్ మూలకాల బాహ్య ఎలక్ట్రాన్ విన్యాసం (n – 2) f1 – 14 (n – 1) d0- 1 ns2
ప్రశ్న 22.
B, Al, Mg, K ల లోహ స్వభావం పెరిగే క్రమాన్ని రాయండి.
జవాబు:
B < Al < Mg < K
ప్రశ్న 23.
B, C, N, F, Si ల సరైన అలోహ స్వభావ పెరుగుదల క్రమాన్ని రాయండి.
జవాబు:
అధిక ఋణ విద్యుదాత్మకత మరియు అధిక అయనీకరణ శక్తి అలోహ ధర్మానికి సూచికలు. పై మూలకాలలో అలోహ స్వభావం Si నుండి F కు పెరుగుతుంది.
Si < B < C < N < F
ప్రశ్న 24.
N, O, F, Cl ల సరైన రసాయన చర్యాశీలత పెరుగుదల క్రమాన్ని వాటి ఆక్సీకరణ ధర్మం పరంగా రాయండి.
జవాబు:
నైట్రోజన్ నుండి ఫ్లోరిన్క ఆక్సీకరణ సామర్థ్యం పెరుగుతుంది. అధిక ఋణ విద్యుదాత్మకత దీనికి కారణం.
N < Cl < O < F
ప్రశ్న 25.
ఋణ విద్యుదాత్మకత అంటే ఏమిటి ? మూలకాల స్వభావాన్ని తెలుసుకోవడానికి ఇది ఎలా ఉపయోగపడుతుంది?
జవాబు:
అణువులోని పరమాణువు బంధ ఎలక్ట్రాన్ జంటను తన వైపుకు ఆకర్షించే సామర్థ్యాన్ని ఋణ విద్యుదాత్మకత అంటారు. అధిక ఋణ విద్యుదాత్మకతను కలిగిన మూలకాలు అధిక అలోహ స్వభావాన్ని చూపుతాయి మరియు బలమైన ఆక్సీకారుణులుగా పనిచేస్తాయి.
ప్రశ్న 26.
పరిరక్షక ప్రభావం అంటే ఏమిటి ? అది ఏ విధంగా అయొనైజేషన్ ఎంథాల్పీ (IE) తో సంబంధం కలిగి ఉంది ?
జవాబు:
వేలన్సీ కక్ష్యకు, కేంద్రకానికీ మధ్యగల కక్ష్యలలోని ఎలక్ట్రాన్లు కేంద్రకావేశాన్ని కొంత వరకు తటస్థీకరించడం వల్ల బాహ్య కక్ష్యలోని ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ తగ్గుతుంది. అంతర్ కక్ష్యలలోని ఎలక్ట్రాన్లు బాహ్య కక్ష్యలలోని ఎలక్ట్రాన్లకు కేంద్రకానికి మధ్యగల ఆకర్షణపై కనబరిచే ఈ ప్రభావాన్ని పరిరక్షక ప్రభావం అంటారు. ఈ ప్రభావం పెరిగితే, అనగా అంతర కక్ష్యల సంఖ్య పెరిగే కొద్దీ అయొనైజేషన్ శక్తి తగ్గుతుంది.

ప్రశ్న 27.
మూలకాల ఋణ విద్యుదాత్మకత లోహ, అలోహ లక్షణాలకు సంబంధం ఏమిటి ?
జవాబు:
ఋణ విద్యుదాత్మకత ఆధారంగా మూలకాల స్వభావాన్ని ఊహించవచ్చు. ఋణ విద్యుదాత్మకత అధికంగా కలిగిన మూలకాలు అలోహ స్వభావాన్ని కలిగి ఉంటాయి. లోహాలకు ఋణ విద్యుదాత్మక విలువలు తక్కువగా ఉంటాయి. ఒక పీరియడ్ మూలకాల్లో ఎడమ నుంచి కుడికి ఋణ విద్యుదాత్మకత పెరుగుతుంది. కనుక లోహ స్వభావము తగ్గి అలోహ స్వభావము పెరుగుతుంది.
ఒక గ్రూపు మూలకాల్లో పై నుంచి కిందకు ఋణ విద్యుదాత్మకత తగ్గుతుంది. కనుక లోహ స్వభావం పై నుండి కిందకు పెరుగుతుంది. అలోహ స్వభావం తగ్గుతుంది.
![]()
ప్రశ్న 28.
ఆక్సిజన్, హైడ్రోజన్ పరంగా ఆర్సినిక్కు సాధ్యమయ్యే వేలన్సీ ఎంత ?
జవాబు:
ఆక్సిజన్ పరంగా ఆర్సినిక్ మూడు మరియు ఐదు సంయోజకతలను చూపుతుంది (As2O3 మరియు As2O5) హైడ్రోజన్ పరంగా AsH3 లో As సంయోజకత మూడు.
ప్రశ్న 29.
ద్విస్వభావిత ఆక్సైడ్ అంటే ఏమిటి ? 13వ గ్రూప్ మూలకం ఏర్పరచే ద్విస్వభావిక ఆక్సైడ్ ఫార్ములాను ఇవ్వండి.
జవాబు:
ఆమ్లాలు మరియు క్షారాలలో చర్యపొందే ఆక్సైడును దిస్వభావ ఆక్సైడ్ అంటారు. 13వ గ్రూపులో Al2O3 మరియు Ga2 O3 లు ద్విస్వభావ ఆక్సైడ్లు.
ప్రశ్న 30.
అధిక ఋణ విద్యుదాత్మకత కల మూలకం ఏది ? దానికి అత్యధిక ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఉందా ? ఎందుకు ఉంది? ఎందుకు లేదు ?
జవాబు:
అధిక ఋణ విద్యుదాత్మకత గలిగిన మూలకం ఫ్లోరిన్ (4.0). కాని ఫ్లోరిన్క అత్యధిక ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ లేదు. హాలోజన్లలో అత్యధిక ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ కలిగిన మూలకం క్లోరిన్. Cl > F > Br > I > At క్రమంలో ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీలు ఉంటాయి.
కారకం : క్లోరిన్ కన్నా ఫ్లోరిన్ చిన్న పరమాణువు కనుక ఫ్లోరిన్పై ఎలక్ట్రాన్ సాంద్రత ఎక్కువ. కొత్తగా చేరే ఎలక్ట్రాన్ . వికర్షణకులోనవుతుంది. అందువల్ల ‘F’ కు ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ విలువ తక్కువ.
F < Cl
ప్రశ్న 31.
కర్ణ సంబంధం అంటే ఏమిటి ? ఈ సంబంధం ఉన్న ఒక మూలకాల జంటను ఇవ్వండి.
జవాబు:
ఒక గ్రూపులో మొదటి మూలకం తరవాత గ్రూపులోని రెండవ మూలకం ఒకే విధమైన ధర్మాలను ప్రదర్శిస్తాయి. దీనిని కర్ణ సంబంధం అంటారు.

Li, Mg లు ఒకే రకమైన ధర్మాలను కలిగి ఉంటాయి.
ప్రశ్న 32.
మూడో పీరియడ్లో ఆక్సైడ్ స్వభావం ఎలా మారుతుంది ?
జవాబు:
ఏ పీరియడ్ మూలకాలలోనైనా ఆక్సెడ్ ఆమ్ల స్వభావం ఎడమ నుంచి కుడికి పెరుగుతుంది. క్షారస్వభావం తగ్గుతుంది. మూడవ పీరియడ్లో ఆక్సైడ్ క్షార స్వభావం తగ్గి ఆమ్ల స్వభావం పెరుగుతుంది.
Na2O నుండి Cl2O7 కు ఆక్సైడ్ స్వభావం మార్పును దిగువ సూచించడమైనది.

ప్రశ్న 33.
ఐరన్ పరమాణువు, వాటి అయాన్ల వ్యాసార్థాలు పాటించే క్రమం Fe > Fe2+ > Fe3+ విశదీకరించండి.
జవాబు:
మాతృ పరమాణువు కన్నా దాని కేటయాన్ చిన్నది. ఒంటరి తటస్థపరమాణువు ఎలక్ట్రాను కోల్పోతే ఏర్పడే ధన అయాన్లో ఎలక్ట్రాన్ల సంఖ్య కన్నా ప్రోటాన్ల ల సంఖ్య ఎక్కువ. అందువల్ల వేలన్సీ ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ అధికమవుతుంది. తత్ఫలితంగా ఎలక్ట్రాన్ మేఘం కుచించుకుపోయి పరిమాణం తగ్గుతుంది.
ఎక్కువ ఎలక్ట్రాన్లను కోల్పోతే అయాన్ పరిమాణం మరింత తగ్గుతుంది. కనుక
Fe > Fe2+ > Fe3+
ప్రశ్న 34.
ఒక మూలకం రెండో అయొనైజేషన్ ఎంథాల్పీ (IE2) కంటే మొదటి అయొనైజేషన్ ఎంథాల్పీ (IE1) తక్కువ. ఎందుకు?
జవాబు:
తటస్థ పరమాణువు ఎలక్ట్రాన్ను కోల్పోయినప్పుడు ఏర్పడే ఏకమాత్ర ధనావేశిత అయాన్లో వేలన్స్ ఎలక్ట్రాన్ల పై కేంద్రక ఆకర్షణ అధికం. అందువల్ల ఎలక్ట్రాను తొలగించుటకు అధిక శక్తి అవసరం అవుతుంది. కనుక ఏక మాత్ర ధనావేశిత అయాన్ నుండి ఎలక్ట్రాను తొలగించుటకు కావలసిన అయొనైజేషన్ పొటెన్షియల్ IE2 విలువ IE1 కంటె ఎక్కువ. అనగా ద్వితీయ అయొనైజేషన్ పొటెన్షియల్ విలువలు ప్రథమ అయొనైజేషన్ పొటెన్షియల్ కన్నా ఎక్కువ.
ప్రశ్న 35.
లాంథనైడ్ సంకోచం అంటే ఏమిటి ? దాని ఫలితాలలో ఒక దానిని చెప్పండి.
జవాబు:
లాంథనైడ్లలో ఎడమ నుంచి కుడికి వాటి పరిమాణాలు క్రమేపి తగ్గుతూ వస్తాయి. Ce నుండి Lu వరకు ఈ తగ్గుదల 0.2 A ఉన్నది. దీనినే లాంథనైడ్ సంకోచం అంటారు.
లాంథనైడ్లలో భేదాత్మక ఎలక్ట్రాన్ (n – 2) f ఉపకక్ష్యలో ప్రవేశిస్తుంది. వితరణం చెందిన ఆకృతుల మూలంగా f – ఆర్బిటాళ్లు, కేంద్ర కాకర్షణ నుండి వేలన్సీ ఎలక్ట్రాన్లకు తగు పరిరక్షణ కల్పించలేవు. ఈ కారణంగా కేంద్రక ఆకర్షణ పెరిగి పరమాణు సైజులు ఎడమ నుండి కుడికి తగ్గుతాయి.
ఈ పరమాణు సైజు తగ్గుదల, లాంథనైడ్ పరమాణువుల కన్నా వాటి +3 అయాన్లలో క్రమ పద్ధతిలో ఉంటుంది.
ఫలితాలు :
- లాంథనైడ్ సంకోచం వలన మూలకాల ద్రవీభవనస్థానం, బాష్పీభవన స్థానం Ce నుండి Lu వరకు పెరుగుతాయి.
- 4d మరియు 5d శ్రేణులలోని గ్రూపుల మూలకాలలో అధిక సారూప్యతలు గోచరిస్తాయి. ఈ సారూప్యత 3d మరియు 4d శ్రేణుల మూలకాలలో కనిపించదు. దీనికి కారణం లాంథనైడ్ సంకోచం.
ఉదా : (Zr, Hf); (Nb, Ta) జంటల పరిమాణాలు దాదాపు సమానం కావున వాటి ధర్మాలలో సారూప్యత ఉంటుంది.
ప్రశ్న 36.
అధిక సంఖ్యలో జతగూడని 2p ఎలక్ట్రాన్లు ఉన్న మూలకం పరమాణు సంఖ్య ఎంత ? అది ఏ గ్రూప్కు చెందింది ?
జవాబు:
p ఆర్బిటాలులో గరిష్ఠంగా 3 జతలేని ఎలక్ట్రాన్లు ఉండవచ్చు. కనుక మూలక ఎలక్ట్రాన్ విన్యాసం 1s2 2s2 2p3 మూలక పరమాణు సంఖ్య 7. మూలకం పేరు నైట్రోజన్. అది Vవ గ్రూప్కు చెందినది.
ప్రశ్న 37.
సోడియంకు బలమైన లోహ స్వభావం ఉంటుంది ? క్లోరిన్క బలమైన అలోహ స్వభావం ఉంటుంది. విశదీకరించండి.
(లేదా)
సోడియం బలమైన లోహం కాగా, క్లోరిన్ బలమైన అలోహం – ఎందుకు ?
జవాబు:
సోడియంకు స్వల్ప అయనీకరణ శక్తి కలదు. అందువల్ల అది ఎలక్ట్రాన్లను సులువుగా కోల్పోయి ధన అయానును ఏర్పరచగలదు. కనుక అది బలమైన లోహ స్వభావము కలిగినది.
క్లోరిన్ కు అధిక ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ మరియు అధిక ఋణ విద్యుదాత్మకతకలవు. అందువల్ల అది సులువుగా ఎలక్ట్రాను గ్రహించి ఋణ అయానును ఏర్పరచగలదు. అందువల్ల అది అధిక అలోహ స్వభావాన్ని కలిగి ఉంటుంది.
ప్రశ్న 38.
శూన్య గ్రూపు మూలకాలను ఉత్కృష్ట లేదా తటస్థ వాయువులని ఎందుకు అంటారు ?
జవాబు:
శూన్య గ్రూపు మూలకాలకు ns2 np6 ఎలక్ట్రాన్ విన్యాసం కలదు. హీలియం ఎలక్ట్రాన్ విన్యాసం 1s2. ఈ ఎలక్ట్రాన్ విన్యాసాలు స్థిరమైనవి. రసాయన జడత్వాన్ని ప్రదర్శిస్తాయి. కనుక వాటిని జడ వాయువులు అంటారు.
ఇటీవల కాలంలో జడ వాయువులు కూడా రసాయనచర్యలలో పాల్గొని సమ్మేళనాలను ఏర్పరుస్తాయి అని కనుగొన్నారు. కాని బంగారం, ప్లాటినం వంటి లోహాల వలె చర్యాశీలత తక్కువని తెలిసినది కనుక వాటిని ఉత్కృష్ట వాయువులని వ్యవహరిస్తారు.
![]()
ప్రశ్న 39.
ప్రతి జంటలో, తక్కువ అయనీకరణ శక్తి ఉన్న దానిని గుర్తించి, కారణాన్ని తెలపండి.
a) I, I–
b) Br, K
c) Li, Li+
d) Ba, Sr
e) O, S
f) Be, B
g) N, O
జవాబు:
a) I– కు అయనీకరణ శక్తి తక్కువ. కారణం : I– పరిమాణం I కంటే ఎక్కువ.
b) K కు అయనీకరణ శక్తి తక్కువ. కారణం : K ధన విద్యుదాత్మక మూలకం కాగా Br ఋణ విద్యుదాత్మక మూలకం.
c) Li కు అయనీకరణ శక్తి తక్కువ. కారణం : Li కు Li+ కంటె పరిమాణం ఎక్కువ.
d) Ba ఒక గ్రూపులో అయనీకరణ శక్తి తగ్గుతుంది. Sr తరువాత మూలకం Ba కనుక Ba అయనీకరణ శక్తి తక్కువ.
e) S కు అయనీకరణ శక్తి తక్కువ. కారణం: Sకు కంటె పరిమాణం ఎక్కువ.
f) B కు అయనీకరణ శక్తి తక్కువ. కారణం : Be లో పూర్తిగా నిండిన ఆర్బిటాళ్ళు ఉంటాయి.
g) O కు అయనీకరణ శక్తి తక్కువ. కారణం : N లో సగం నిండిన ఆర్బిటాళ్ళు ఉంటాయి.
ప్రశ్న 40.
ఆక్సిజన్ IE1 < నైట్రోజన్ IE1 కాని ఆక్సిజన్ IE2 > నైట్రోజన్ IE2 – విశదీకరించండి.
జవాబు:

‘N’ లో సగం నిండిన ‘p’ ఆర్బిటాళ్ళు ఉన్నాయి కాబట్టి దాని IE1 ‘O’ యొక్క IE1 కన్నా తక్కువగా ఉంటుంది.
‘O+‘ లో సగం నిండిన ‘p’ ఆర్బిటాళ్ళు ఉన్నాయి కాబట్టి దాని IE2 ‘O’ యొక్క IE2 కన్నా ఎక్కువగా ఉంటుంది.
ప్రశ్న 41.
Na+, Ne లకు ఒకే ఎలక్ట్రాన్ విన్యాసం ఉన్నప్పటికీ, Nat కు Ne కంటే ఎక్కువ అయనీకరణ శక్మపు విలువను కలిగి ఉంది – విశదీకరించండి.
జవాబు:
Na+ అయాన్ కేంద్రకంలో ప్రోటానుల సంఖ్య (11) Ne పరమాణువు కేంద్రకంలోని ప్రోటానుల సంఖ్య (10) కంటే ఎక్కువ. Na+, Ne, లలో ఎలక్ట్రానుల సంఖ్య సమానం. కాని Nat కేంద్రకం ఎలక్ట్రానులను బలంగా ఆకర్షిస్తుంది. కనుక Na+ I.P విలువ Ne కంటే ఎక్కువ.
ప్రశ్న 42.
కింది ప్రతి జంటలో దేనికి ఎక్కువ రుణాత్మక ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఉంది ? విశదీకరించండి.
a) N, O
b) F, Cl
జవాబు:
a) ఆక్సిజన్ కు ఎక్కువ. నైట్రోజన్లో p3 ఎలక్ట్రాన్ విన్యాసం స్థిరమైనది కనుక దాని ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఆక్సిజన్ కన్నా తక్కువ.
b) క్లోరిన్కు ఎక్కువ: ఫ్లోరిన్ స్వల్ప పరిమాణం కారణంగా అధిక ఎలక్ట్రాన్ సాంద్రతను కలిగి, కొత్తగా చేరే ఎలక్ట్రాన్ అధిక వికర్షణకు గురవుతుంది. అందువల్ల విడుదలయ్యే ఉష్ణం తక్కువ. ఫ్లోరిన్ E.A. తక్కువ.
ప్రశ్న 43.
క్లోరిన్ ఎలక్ట్రాన్ అఫినిటి ఫ్లోరిన్ కంటే ఎక్కువ – విశదీకరించండి.
జవాబు:
ఫ్లోరిన్ స్వల్ప పరిమాణం వల్ల దానిపై ఎలక్ట్రాన్ సాంద్రత ఎక్కువ. అందువల్ల కొత్తగా చేరే ఎలక్ట్రాన్ వికర్షణకు లోనవుతుంది. వికర్షణను అధిగమించడానికి విడుదలయ్యే ఉష్ణంలో కొంత ఖర్చుచేయబడుతుంది. అందువల్ల ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ తగ్గుతుంది. క్లోరిన్ పరిమాణం అధికం కనుక ఈ విధమైన వికర్షణలు ఉండవు. కనుక క్లోరిన్ ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్చీ ఎక్కువ. ఫ్లోరిన్క తక్కువ.
ప్రశ్న 44.
కింది ప్రతి జంటలో దేనికి ఎక్కువ ఎలక్ట్రాన్ అఫినిటీ ఉంది ?
a) F, Cl–
b) O, O–
c) Na+, F
d) F, F–
జవాబు:
a) F
b) O
c) Na+
d) F
ప్రశ్న 45.
కింది వాటిని అయానిక వ్యాసార్ధ పెరుగుదల క్రమంలో అమర్చండి.
a) Cl–, P-3, S-2, F–
b) Al+3, Mg++, Na+, O-2, F–
c) Na+, Mg++, K+
జవాబు:
a) F– < Cl– < S-2 < P-3
b) Al+3 < Mg++ < Na+ < F– < O-2
c) Mg++ < Na+ < K+
ప్రశ్న 46.
Mg++, O-2 రెండూ ఒకే ఎలక్ట్రాన్ విన్యాసాన్ని కలిగి ఉన్నప్పటికీ, పరిమాణంలో Mg++, O-2 కంటే తక్కువ.
జవాబు:
Mg++ మరియు O-2 లు సమ ఎలక్ట్రాన్ సంఖ్య కలిగినవి. కాని Mg++ లో ప్రోటానుల సంఖ్య (12) O-2 (8) లో కన్న ఎక్కువ. అందువల్ల Mg++ లో కేంద్రక ఆకర్షణా ప్రభావం O-2 లో కన్నా ఎక్కువ. అందువల్ల Mg++ అయాను పరిమాణం తక్కువగా ఉంటుంది.
ప్రశ్న 47.
B, Al, C, Si మూలకాలలో
a) దేనికి అత్యధిక ప్రథమ అయొనైజేషన్ ఎంథాల్పీ ఉంది ?
b) దేనికి ఎక్కువ రుణాత్మక ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఉంది ?
c) దేనికి అత్యధిక పరమాణు వ్యాసార్ధం ఉంది ?
d) దేనికి ఎక్కువ లోహ స్వభావం ఉంది ?
జవాబు:
a) C
b) C
c) Al
d) Al
ప్రశ్న 48.
N, P, O, S మూలకాలను గమనించండి. వాటిని
a) ప్రథమ అయొనైజేషన్ ఎంథాల్పీ పెరుగుదల క్రమంలో
b) ఋణాత్మక ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ పెరుగుదల క్రమంలో
c) అలోహ స్వభావం పెరిగే క్రమంలో రాయండి.
జవాబు:
a) S < P < O < N
b) N < P < O < S
c) P < N < S < O
ప్రశ్న 49.
ఇచ్చిన క్రమంలో అమర్చండి :
a) ఎలక్ట్రాన్ గ్రాహ్య (EA) పెరుగుదల : O, S, Se
b) IE1 పెరుగుదల : Na, K, Rb
c) వ్యాసార్ధం పెరుగుదల : I–, I+, I
d) రుణ విద్యుదాత్మకత పెరుగుదల : F, Cl, Br, I
e) EA పెరుగుదల : F, Cl, Br, I
f) వ్యాసార్ధం పెరుగుదల : Fe, Fe+2, Fe+3
జవాబు:
a) O < Se < S
b) Rb < K < Na c) I,sup>+ < I, < I–
d) I < Br < Cl < F
e) I < Br < F< Cl
f) Fe+3 < Fe+2 < Fe
ప్రశ్న 50.
a) అత్యధిక అయొనైజేషన్ ఎంథాల్పీ ఉన్న మూలకం ఏది ?
b) అత్యధిక అయొనైజేషన్ ఎంథాల్పీ విలువ గల గ్రూపు ఏది ?
c) అత్యధిక ఎలక్ట్రాన్ అఫినిటీని చూపే మూలకం ఏది ?
d) మెండలీవ్ కాలానికి తెలియని మూలకాల పేర్లు ఏమిటి ?
e) ఏవైనా రెండు ప్రాతినిధ్య మూలకాల పేర్లు తెలపండి.
జవాబు:
a) హీలియం
b) శూన్య గ్రూపు
c) క్లోరిన్
d) ఏకా బోరాన్ – గాలియం
ఏకా అల్యూమినియం – స్కాండియం
ఏ సిలికాన్ – జర్మేనియం
e) సోడియం మరియు మెగ్నీషియం
![]()
ప్రశ్న 51.
a) ఏవైనా రెండు వారధి మూలకాల పేర్లు తెలపండి.
b) కర్ణ సంబంధం చూపే ఏదైనా రెండు జంటలను తెలపండి.
c) రెండు పరివర్తన మూలకాల పేర్లు తెలపండి.
d) రెండు విరళ మృత్తిక మూలకాల పేర్లు తెలపండి.
e) రెండు ట్రాన్స్ యురానిక్ మూలకాల పేర్లు తెలపండి.
జవాబు:
a) సోడియం మరియు మెగ్నీషియం
b) Li, Mg; Be, Al
c) క్రోమియం మరియు కాపర్
d) సీరియం మరియు లుటేషియం
e) నెప్ట్యూనియం మరియు ప్లుటోనియం
లఘు సమాధాన ప్రశ్నలు
ప్రశ్న 52.
ఆవర్తన పట్టికలోని 6వ పీరియడ్లో 32 మూలకాలు ఉన్నాయని, క్వాంటమ్ సంఖ్యల ఆధారంతో సమర్థించండి.
జవాబు:
విస్తృత ఆవర్తనా పట్టికలో ప్రతి పీరియడ్లో కొత్త ప్రధాన శక్తి స్థాయిలో ఎలక్ట్రాన్లు ప్రవేశిస్తాయి. 6వ పీరియడ్ మూలకాలలో 6వ శక్తి స్థాయిలో ఎలక్ట్రాన్లు ప్రవేశిస్తాయి. 6వ పీరియడ్లో చివరి మూలకం ఎలక్ట్రాన్ విన్యాసం 6s2 6p6. 6p ఉపస్థాయి నిండుటకు ముందు 6s, 4f, 5d లలో ఎలక్ట్రాన్లు ప్రవేశిస్తాయి. 6s లో రెండు, 40 లో పద్నాలుగు, 5d లో పది, మరియు 6p లో ఆరు, మొత్తం 32 ఎలక్ట్రాన్లు ప్రవేశిస్తాయి. కనుక 6వ పీరియడ్లో మొత్తం మూలకాల సంఖ్య 32.
ప్రశ్న 53.
పరమాణు భారం కంటె పరమాణు సంఖ్య మూలకాల ప్రాథమిక ధర్మమని, పరమాణు సంఖ్యలపై మేస్లే జరిపిన కృషి ఎలా తెలుపుతుంది ?
జవాబు:
1913 సం||లో మోస్లే మూలకాల X – కిరణ వర్ణ పటంను తయారుచేసాడు. దీన్ని బట్టి మూలక పరమాణు కేంద్రకం పై గల ఆవేశానికి అది వెలువరించిన X కిరణాల పౌనః పున్యానికి సంబంధం ఉందని చూపాడు.

\(\sqrt{v}\) = a (Z – b) సమీకరణంలో
υ = x – వికిరణాల పౌనః పున్యం,
Z = మూలకం కేంద్రక ఆవేశం, దీన్నే పరమాణు సంఖ్య అన్నారు.
a, b, లు x కిరణాల స్థిరాంకాలు.
\(\sqrt{v}\) . z ల మధ్య గీసిన రేఖాపటం ఒక సరళ రేఖగా ఉన్నది. ఇదే రకమైన సంబంధము, \(\sqrt{v}\) పరమాణు భారాల మధ్య కనబడలేదు. దీన్ని బట్టి, పరమాణు భారం గాక, పరమాణు సంఖ్య మూలకం యొక్క మెరుగైన మౌలిక లక్షణమని తెలుస్తున్నది. X – కిరణాల పౌనః పున్యము, పరమాణువులోపలి నిర్మాణం పైన అనగా ఎలక్ట్రాన్ల సంఖ్య పైన ఆధారపడుతుంది. ఆ సంఖ్యయే పరమాణు సంఖ్య.
ప్రశ్న 54.
ఆధునిక ఆవర్తనా నియమాన్ని తెలపండి. విస్తృత ఆవర్తన పట్టికలో ఎన్ని గ్రూప్లు, పీరియడ్లు ఉన్నాయి ?
జవాబు:
‘మూలకాల భౌతిక, రసాయన ధర్మాలు వాటి పరమాణు సంఖ్యల ఆవర్తన ప్రమేయాలు’. విస్తృత ఆవర్తన పట్టికలో 18 గ్రూపులు, 7 పీరియడ్లు ఉన్నాయి.
ప్రశ్న 55.
f – బ్లాక్ మూలకాలను అసలు పట్టిక కింద ఎందుకు అమర్చారు ?
జవాబు:
f బ్లాకు మూలకాలను ప్రధాన పట్టికలోనే ఉంచాలంటే ఆవర్తన పట్టిక పరిమాణం పెరుగుతుంది. దీనిని నివారించుటకు f బ్లాకు మూలకాలను అసలు పట్టిక క్రింద అమర్చారు.
లాంథనైడ్లలో 4f స్థాయి క్రమేపి నిండుతుంది. ఆక్టినైడ్లలో 51 స్థాయి క్రమేపి నిండుతుంది. సారూప్య ధర్మాలు గల మూలకాలను ఒకే నిలువు పట్టీలో ఉంచాలనే వర్గీకరణ సూత్రం అమలు అయ్యేటట్లు,, ఆవర్తన పట్టిక నిర్మాణాన్ని చేయడానికి 4f, 5f అంతర పరివర్తన శ్రేణుల మూలకాలను ఆవర్తన పట్టికలో వేరుగా ఉంచారు.
ప్రశ్న 56.
విస్తృత ఆవర్తన పట్టికలోని ప్రతి పీరియడ్లో ఉన్న మూలకాల సంఖ్యను తెలపండి.
జవాబు:
మొదటి పీరియడ్ – 2 మూలకాలు
రెండవ పీరియడ్ – 8 మూలకాలు
మూడవ పీరియడ్ – 8 మూలకాలు
నాల్గవ పీరియడ్ – 18 మూలకాలు
ఐదవ పీరియడ్ – 18 మూలకాలు
ఆరవ పీరియడ్ – 32 మూలకాలు
ఏడవ పీరియడ్ – 29 మూలకాలు
ప్రశ్న 57.
కింద వాటి సాధారణ బాహ్య కక్ష్య ఎలక్ట్రాన్ విన్యాసాలను తెలపండి.
a) ఉత్కృష్ట వాయువులు
b) ప్రాతినిధ్య మూలకాలు
c) పరివర్తన మూలకాలు
d) అంతర పరివర్తన మూలకాలు
జవాబు:
a) జడవాయువులు : ns2 np6 (ns2 for He)
b) ప్రాతినిథ్య మూలకాలు : ns1 – 2 ns0 – 5
c) పరివర్తన మూలకాలు : (n – 1) d1 – 10 ns1 – 2
d) అంతర పరివర్తన మూలకాలు : (n – 2)f1 – 14 (n – 1) d0 – 1 ns2
ప్రశ్న 58.
పరివర్తన మూలకాల ఏవైనా నాలుగు అభిలాక్షణిక ధర్మాలను తెలపండి.
జవాబు:
పరివర్తన మూలకాల అభిలాక్షణిక ధర్మాలు.
- పరివర్తన మూలకాలు కఠిన మరియు బరువైన లోహాలు
- అధిక సాంద్రత, ద్రవీభవన, బాష్పీభవన ఉష్ణోగ్రతలు
- ఉత్తమ ఉష్ణ మరియు విద్యుత్ వాహకాలు
- అనేక ఆక్సీకరణ స్థితులు చూపుట
- రంగు కలిగిన సమ్మేళనాలను ఏర్పరుచుట
- పారా అయస్కాంత ధర్మం
- సంక్లిష్ట సమ్మేళనాలను ఏర్పరుచుట.
ప్రశ్న 59.
విరళ మృత్తిక లోహాలు, ట్రాన్స్ యురానిక్ మూలకాలు అంటే ఏమిటి ?
జవాబు:
సీరియం (Z = 58) నుండి లుటీషియం వరకు గల 14 మూలకాలు భూమిలో లభ్యత తక్కువ. కనుక వీటిని విరళ మృత్తికలు అంటారు. వీటి ధర్మాలు లాంథనంను పోలి ఉంటాయి కనుక లాంథనైడ్లు అని కూడా అంటారు. వీటిని 4f శ్రేణి మూలకాలంటారు.
యురేనియం (z = 92) తరువాత మూలకాలను ట్రాన్స్ యురానిక్ మూలకాలు అంటారు. ఈ మూలకాలు ప్రకృతిలో లభించవు. అవి సంశ్లేషిత మూలకాలు. అవి రేడియోధార్మిక మూలకాలు. ఇవి 5f శ్రేణి మూలకాలు.
ప్రశ్న 60.
సమ ఎలక్ట్రానిక్ శ్రేణులంటే ఏమిటి ? కింద ఉన్న ప్రతి పరమాణువు, అయాన్లకు సంబంధించిన సమ ఎలక్ట్రానిక్ శ్రేణులను తెలపండి.
(a) F–
b) Ar
c) He
d) Rb+
జవాబు:
సమాన సంఖ్యలో ఎలక్ట్రాన్లను కలిగిన అయానులను సమ ఎలక్ట్రానిక్ శ్రేణి అంటారు.
a) N-3, O-2, F–, Na+, Mg++, Al+++
b) P-3, S-2, Cl–, K+, Ca++, Sc3+
c) H–, He, Li+, Be++
d) As3-, Se2-, Br–, Rb,sup>+, Sr2+
ప్రశ్న 61.
వ్యాసార్ధంలో మాతృక పరమాణువుల కంటే ఎందుకు కాటయాన్ చిన్నగా ఉంటుందో, ఆనయాన్ పెద్దగా ఉంటుందో విశదీకరించండి.
జవాబు:
తటస్థ పరమాణువు నుంచి ఒక ఎలక్ట్రాను తొలగించినపుడు, కాటయాన్ ఏర్పడుతుంది. కాటయాను మరియు దాని పరమాణువులకు కూడా కేంద్రక ఆవేశం సమానమే. కాని కాటయానులోని ఎలక్ట్రాన్ల సంఖ్య, మాతృపరమాణువులో కన్నా తక్కువగా ఉంటాయి. ఆ కారణంగా కేంద్రక ఆకర్షణ ఎలక్ట్రాన్లపై పెరిగి ఎలక్ట్రాన్ మేఘం సంకోచిస్తుంది. కాబట్టి కాటయాన్ సైజు తగ్గుతుంది.

తటస్థ పరమాణువుకు ఎలక్ట్రాన్ను చేర్చినప్పుడు, ఆనయాన్ ఏర్పడుతుంది. ఆనయాన్ మరియు దాని మాతృపరమాణువులోను కేంద్రక ఆవేశం సమానమే. కాని ఆనయానులోని ఎలక్ట్రాన్ల సంఖ్య, మాతృ పరమాణువులో కన్నా అధికంగా ఉంటాయి. ఆ కారణంగా కేంద్రక ఆకర్షణ ఎలక్ట్రాన్లపై తగ్గి ఎలక్ట్రాన్ మేఘం వ్యాకోచిస్తుంది. కాబట్టి ఆనయాన్ సైజు పెరుగుతుంది.
![]()
ప్రశ్న 62.
రెండవ పీరియడ్ మూలకాలను, వాటి ప్రథమ అయొనైజేషన్ ఎంథాల్పీలు పెరిగే క్రమంలో అమర్చండి. B కంటే Be కు అధిక IE1 ఎందుకు ఉందో తెలపండి.
జవాబు:
Li < B < Be < C < O < N < F
Be ఎలక్ట్రాన్ విన్యాసం 1s2 2s2. దీనిలో బాహ్యతమ ఎలక్ట్రాన్ జతకూడి ఉన్నది. అంతేగాక, బాగా చొచ్చుకుపోయే S ఆర్బిటాల్లో ఉన్నది. అనగా దాన్ని పరమాణువు నుండి విడదీయడానికి అధిక శక్తి కావాలి. అనగా అధిక IP అవసరము. B ఎలక్ట్రాన్ విన్యాసం 1s2 2s2 2p1. దానిలో బాహ్యతమ ఎలక్ట్రాన్ ఒంటరిగా ఉన్నది మరియు తక్కువగా చొచ్చుకుపోయే p ఆర్బిటాల్లో ఉన్నది. కాబట్టి B అయనీకరణ శక్తి తక్కువ. కాబట్టి Be కంటే B కి తక్కువ IP ఉన్నది.
ప్రశ్న 63.
Mg కంటె Na IE1 తక్కువ, కానీ Mg కంటే Na IE2 ఎక్కువ – విశదీకరించండి.
జవాబు:
Mg 1s2 2s2 2p6 3s2 లోని 3s ఎలక్ట్రాన్లు జంటగా ఉన్నాయి. (3s2) కాబట్టి బాహ్యతమ ఎలక్ట్రాన్, అనగా 3s ఎలక్ట్రాన్ జత గూడి ఉన్నది. అదీ గాక ఆ ఎలక్ట్రాన్ అధికంగా చొచ్చుకుపోయే s ఆర్బిటాల్లో ఉన్నది. కాబట్టి ఈ 3s ఎలక్ట్రాను తొలగించటానికి అధికశక్తి అవసరము. కాబట్టి Mg కు అయనీకరణశక్తి ఊహించిన దాని కన్నా అధికంగా ఉంటుంది.
Na+ అయానుకు స్థిరమైన 2s22p6 ఎలక్ట్రాన్ విన్యాసం కలదు. అందువల్ల Na+ నుండి ఎలక్ట్రాను తొలగించుటకు అధిక శక్తి అవసరము. అనగా Na కు IE2 విలువ ఎక్కువగా ఉంటుంది. Mg+ కు స్థిర ఎలక్ట్రాన్ విన్యాసం లేదు కనుక Mg IE2 విలువ తక్కువ.
ప్రశ్న 64.
ప్రాతినిధ్య గ్రూప్ మూలకాల IE గ్రూప్లో కిందకు తగ్గడానికి గల కారణాలు ఏమిటి ?
జవాబు:
ఒక గ్రూపులో పై నుండి క్రిందకి పోయే కొద్దీ పరమాణు సైజు పెరుగుతుంది. కనుక అయనీకరణ శక్తి తగ్గుతుంది. గ్రూపులో కేంద్రకావేశం పెరిగినా కూడా దానితోబాటు అంతర కక్ష్యల సంఖ్య పెరిగి ఆ కక్ష్యల పరిరక్షక ప్రభావం పెరుగుతుంది. అదీకాక పరమాణు సైజు పెరుగుతుంది. కాబట్టి బాహ్యతమ ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ తగ్గుతుంది. అందువల్ల ఎలక్ట్రాన్ను తేలికగా తీసివేయవచ్చు. అంటే అయనీకరణ శక్తి గ్రూపులో క్రిందికి తగ్గుతుంది.
ప్రశ్న 65.
13వ గ్రూప్ మూలకాల ప్రథమ అయొనైజేషన్ ఎంథాల్పీ విలువలు (KJ Mol-1) లలో

సాధారణ క్రమం నుంచి ఈ విచలనాన్ని ఏ విధంగా విశదీకరిస్తారు ?
జవాబు:
B నుండి Al కు అయొనైజేషన్ విలువలో తగ్గుదలకు కారణం పరమాణు పరిమాణం పెరగడమే. ప్రథమ పరివర్తనా శ్రేణి మూలకాల తర్వాత గాలియం వస్తుంది. గాలియంలోని 3d ఎలక్ట్రానులకు పరిరక్షక ప్రభావం తగ్గుతుంది. అందువల్ల పరమాణు పరిమాణం తగ్గుతుంది. ఈ కారణంగా Al, Ga లు సమాన సైజు కలిగి ఉంటాయి. ఇదే విధంగా ఇండియంలో 4d ఎలక్ట్రానులకు కూడా పరిరక్షక ప్రభావం తక్కువ.
అందువల్ల Al, Ga మరియు ln లకు అయనీకరణ శక్తి దాదాపుగా సమానంగా ఉంటుంది. టాలియంలో 5d ఎలక్ట్రానులతోపాటు 4f ఎలక్ట్రానులు కూడా ఉంటాయి. 4f ఎలక్ట్రానులకు పరిరక్షక ప్రభావం తక్కువ. అందువల్ల టాలియం పరిమాణం తగ్గుతుంది. ఈ కారణంగా Tl అయనీకరణ శక్తి Al, Ga, In ల కన్న ఎక్కువ.
ప్రశ్న 66.
ఆక్సిజన్ రెండవ ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ, మొదటి ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ కంటె ధనాత్మకమా ? ఎక్కువ ఋణాత్మకమా? లేదా తక్కువ ఋణాత్మకమా ? సమర్ధించండి.
జవాబు:
ఆక్సిజన్ మొదటి ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఋణాత్మకం. అంటే అవి : 1 ఎలక్ట్రాన్ను గ్రహించినప్పుడు శక్తి విడుదలవుతుంది. అనగా ΔH విలువ ఋణ గుర్తు కలిగి ఉంటుంది. ఏర్పడిన ఋణ అయానుకు మరొక ఎలక్ట్రాన్ కలుపవలెనన్న, ఋణావేశానికి, కలిపెడి ఎలక్ట్రాన్కు మధ్య వికర్షణలు అధికంగా ఉండి దాన్ని నిరోధిస్తాయి. కాబట్టి X– అయానుకు మరొక ఎలక్ట్రాను కలుపవలెనన్న శక్తి అవసరమవుతుంది. అనగా ΔH విలువ ధనాత్మకమవుతుంది. అనగా EA2 విలువ గ్రహించిన శక్తి అవుతుంది.
O + e– → O–; ΔH = – 142 KJ mol-1
\(\overline{\mathrm{o}}\) + e– → O2-; ΔH =+ 702 KJ mol-1
ప్రశ్న 67.
ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ, ధన విద్యుదాత్మకతల మధ్య ప్రాథమికమైన తేడా ఏమిటి ?
జవాబు:
వాయుస్థితిలోని ఒంటరి తటస్థ పరమాణువు ఒక ఎలక్ట్రాన్ ను గ్రహించినప్పుడు విడుదలయ్యే శక్తిని ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ అంటారు.
X(g) + e– → \(\mathrm{x}_{(\mathrm{g})}^{-}\) ; ΔH = -ve
ధనవిద్యుదాత్మకత ఎలక్ట్రాన్ కోల్పోయే స్వభావాన్ని తెలుపుతుంది. లోహాలు ఎలక్ట్రాన్ కోల్పోయి ధన అయాన్లుగా మారతాయి.
ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఎక్కువగా ఉన్న మూలకాలకు ఎలక్ట్రాన్ గ్రహించే స్వభావం ఉంటుంది. అటువంటి మూలకాలు అలోహ ధర్మాలను చూపుతాయి.
అధిక ధన విద్యుదాత్మకత మూలకాలు బలమైన క్షయకారుణులుగాను, ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీలు అధికంగా ఉన్న మూలకాలు ఆక్సీకారుణులు గాను ప్రవర్తిస్తాయి.
ప్రశ్న 68.
ఒకే మూలకపు రెండు ఐసోటోప్లు IE1 లు ఒకేలా ఉంటాయో లేదో ఊహించగలరా ? సమర్థించండి.
జవాబు:
ఒక మూలకపు ఐసోటోపులు ఒకే IE విలువలను కలిగి ఉంటాయి. ఐసోటోపుల పరమాణు సంఖ్యలు సమానం కనుక అవి ఒకే కేంద్రక ఆవేశాన్ని కలిగి ఉంటాయి. వాటి పరమాణు పరిమాణాలు సమానం. కనుక ఐసోటోపులలోని ఎలక్ట్రానులపై కేంద్రక ఆకర్షణ సమానం. కనుక ఐసోటోపుల IE1 లు సమానం.
![]()
ప్రశ్న 69.
గ్రూప్ 1 మూలకాల చర్యాశీలత పెరిగే క్రమం Li < Na < K < Rb <Cs, అయితే గ్రూప్ 17 మూలకాలకు ఈ క్రమం F > Cl > Br > I. విశదీకరించండి.
జవాబు:
గ్రూప్ I మూలకాల ధర్మాలు ధనవిద్యుదాత్మకత మీద ఆధారపడినవి. ఇవి లోహాలు. లోహ స్వభావం Li నుండి Cs కు పెరుగుతుంది. దీనికి కారణం Li నుండి Cs కు అయనీకరణశక్తి తగ్గడమే.
Li < Na < K < Rb < Cs గ్రూపు 17 మూలకాలు హాలోజన్లు. ఇవి అలోహాలు. వీటి ధర్మాలు ఋణ విద్యుదాత్మకత పై ఆధారపడినవి. ఇవి ఎలక్ట్రాను గ్రహించి ఋణ అయాన్ గా మారతాయి. ఫ్లోరిన్క ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ తక్కువయినప్పటికి, ఋణ విద్యుదాత్మకత విలువ ఎక్కువ. అధిక ఋణ విద్యుదాత్మకత మరియు ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీలు అధికంగా ఉన్నందువల్ల హాలోజన్లు అధిక చర్యాశీలత కలవి. కాని ఈ విలువలు F నుండి I కు తగ్గడం వల్ల చర్యాశీలత F నుండి 1 కు తగ్గుతుంది. F > Cl > Br > I
ప్రశ్న 70.
కింద ఇచ్చిన బాహ్య ఎలక్ట్రాన్ విన్యాసం గల మూలకం స్థానాన్ని తెలపండి.
a) ns2 np4 (n = 3)
b) (n − 1) d2 ns2 (n = 4)
జవాబు:
a) 3s2 3p4 (n = 3)
n = 3 అయితే మూలకం మూడవ పీరియడ్కు చెందుతుంది. బాహ్యకర్పరంలో ఆరు ఎలక్ట్రాన్లు ఉన్నాయి కనుక అది 6వ గ్రూపు మూలకం. మూలకం సల్ఫర్.
b) 3d2 4s2 (n = 4) n = 4 కనుక మూలకం 4వ పీరియడ్కు చెందినది. (n – 1)d ఆర్బిటాల్లో రెండు ఎలక్ట్రాన్లు ఉన్నాయి కాబట్టి అది d బ్లాకుకు చెందినది. బాహ్య విన్యాసం 3d2 4s2 మూలకం Titanium. గ్రూపు IV B.
ప్రశ్న 71.
కింద ఉన్న జంట మూలకాల కలయికతో ఏర్పడగల స్థిర యుగ్మ సమ్మేళనాల ఫార్ములాలను నిర్దేశించండి.
a) Li, O
b) Mg, N
c) Al, I
d) Si, O
e) P, Cl
f) పరమాణు సంఖ్య 30 గల మూలకం, Cl
జవాబు:
a) లిథియం వేలన్సీ 1. ఆక్సిజన్ వేలన్సీ 2. కనుక సమ్మేళనం ఫార్ములా Li2O
b) మెగ్నీషియం వేలన్సీ 2. నైట్రోజన్ వేలన్సీ 3. కనుక ఫార్ములా Mg3N2
c) అల్యూమినియం వేలన్సీ 3. అయొడిన్ వేలన్సీ 1. ఫార్ములా AlI3
d) సిలికాన్ వేలన్సీ 4. ఆక్సిజన్ వేలన్సీ 2. ఫార్ములా SiO2
e) ఫాస్ఫిరస్ వేలన్సీలు 3 మరియు 5. కాని +3 ఆక్సీకరణ స్థితి స్థిరమైనది. ఫార్ములా PCl3
f) Z = 30 గల మూలకం Zn. దీని వేలన్సీ 2. ఫార్ములా ZnCl2
ప్రశ్న 72.
గ్రూప్ , పీరియడ్లో లోహ స్వభావంలో మార్పుపై వివరణ ఇవ్వండి.
జవాబు:
ఎలక్ట్రాన్లను వదలుకొని ధనావేశిత అయానులను (కాటయాన్లు) ఏర్పరచే మూలకాన్ని లోహం అంటారు.
గ్రూపులో : పై నుండి క్రిందకు వెళ్లితే, ఎలక్ట్రాన్లు కోల్పోయి ధనావేశ అయాన్లుగా మారే స్వభావం పెరుగుతుంది. అంటే లోహ స్వభావం పెరుగుతుంది. లేదా అలోహ స్వభావం తగ్గుతుంది. దీనికి కారణం, గ్రూపులో పరమాణు సైజు పై నుండి క్రిందకు పెరగడమే. పరమాణు సైజు పెరిగే కొద్దీ, అయనీకరణ శక్తి తగ్గి పరమాణువు సులభంగా ఎలక్ట్రాన్లు కోల్పోయి కాటయాన్ మారుతుంది. అనగా లోహ స్వభావం పెరుగుతుంది.
ప్రతి పీరియడ్ బలమైన లోహం (క్షారలోహం)తో మొదలై, బలమైన అలోహం (హాలోజన్)తో అంతమవుతుంది. అంటే పీరియడ్లో ఎడమ నుండి కుడికి వెళ్లిన కొద్దీ మూలకాలలో లోహ ధర్మం తగ్గి అలోహ ధర్మం పెరుగుతుంది.
కారణం : పరమాణు సంఖ్య పెరిగే కొద్దీ, పీరియడ్లో ఎడమ నుండి కుడికి పరమాణు సైజు తగ్గుతుంది. కాబట్టి అయనీకరణ శక్తి పెరిగి, మూలకం ఎలక్ట్రానులను సులభంగా కోల్పోదు. అది ఎలక్ట్రాన్లను పొందడానికి అపేక్ష కనబర్చుతుంది. అంటే లోహతత్వం తగ్గి అలోహతత్వం పెరుగుతుంది.
ప్రశ్న 73.
గ్రూప్ – 7లో కోవలెంట్ వ్యాసార్థం ఏ విధంగా పెరుగుతుంది ?
జవాబు:
పరివర్తన మూలకాలలో 7వ గ్రూపు మూలకాలైన మాంగనీస్, టెక్నీషియం మరియు రీనియం (Manganese, technicium and Rhenium) లలో సమయోజనీయ వ్యాసార్ధం Mn to Tc కు పెరుగుతుంది. మాంగనీసులో బాహ్య కర్పరం నాలుగు టెక్నిషియంలో బాహ్య కర్పరం 5. కక్ష్యల సంఖ్య టెక్నీషియం (technicium) నుండి రీనియం (Rhenium) కు 5 నుండి 6కు పెరుగుతుంది. కాని లాంథనైడ్ సంకోచం కారణంగా Tc, Re లకు దాదాపు సమాన వ్యాసార్థం ఉంటుంది.
ప్రశ్న 74.
3వ పీరియడ్లో ఏ మూలకానికి అత్యధిక IE1 ఉన్నది ? ఈ పీరియడ్లో IE1 లో మార్పును విశదీకరించండి.
జవాబు:
ప్రతి పీరియడ్లోను చివరి మూలకానికి అనగా జడవాయు మూలకానికి అత్యధిక అయొనైజేషన్ పొటెన్షియల్ ఉంటుంది. కనుక ఆ మూలకం ఆర్గాన్.
3వ పీరియడ్లో IE1 మార్పు : 3వ పీరియడ్లో IE1 పెరిగే క్రమం Na < Al < Mg < Si < P < Cl < Ar
Mg కు IE1 విలువ AI IE1 కన్నా ఎక్కువ :
కారణం : మెగ్నీషియం ఎలక్ట్రాన్ విన్యాసం 1s2 2s2 2p6 3s2 బాహ్య కర్పరంలో 3s ఆర్బిటాల్లోని ఎలక్ట్రానులు జతకూడినవి. అంతేకాక S – ఆర్బిటాల్లోని ఎలక్ట్రాన్లకు చొచ్చుకుపోయే సామర్థ్యం (Penetrating power) ఎక్కువ. అందువల్ల ఆ ఎలక్ట్రాన్ను తొలగించడానికి అధిక శక్తి అవసరం. కనుక Mg కు IE1 ఎక్కువ.
సల్ఫర్ కన్నా ఫాస్ఫరస్ IE1 ఎక్కువ : ఫాస్ఫరస్ ఎలక్ట్రాన్ విన్యాసం 1s 2s2 2p6 3s2 \(3 p_x^1 3 p_y^1 3 p_z^1\) సగం నిండిన ఆర్బిటాల్ ఉండుట వలన ఆ ఎలక్ట్రాన్ విన్యాసం స్థిరమైనది. అందువల్ల ఫాస్ఫరస్ IE1 ఎక్కువ.
ప్రశ్న 75.
మూలకం సంయోజకత (valency) అంటే ఏమిటి ? మూడో పీరియడ్లో హైడ్రోజన్ పరంగా ఇది ఎట్లా మారుతుంది?
జవాబు:
‘సంయోజకత’ (వేలన్సీ) అనగా ‘కలయిక శక్తి’. ఎన్ని హైడ్రోజన్ పరమాణువులతో లేదా ఎన్ని క్లోరిన్ పరమాణువులతో మూలకపు ఒక పరమాణువు సంయోగం చెందుతుందో, ఆ సంఖ్యను ఆ మూలకపు వేలన్సీ అవుతుంది.
ఉదా : NH3 లో ఒక నైట్రోజన్ పరమాణువు, మూడు H లతో సంయోగం చెందింది కాబట్టి N యొక్క సంయోజకత = 3.
ఒకే గ్రూపులోని మూలకాలన్నీ సాధారణంగా ఒకే వేలన్సీ కల్గి ఉంటాయి.
‘s’ బ్లాకు మూలకాల వేలన్సీ = గ్రూపు సంఖ్య
p బ్లాకు మూలకాల వేలన్సీ = గ్రూపు సంఖ్య లేదా (8 – గ్రూపు సంఖ్య)
హైడ్రోజన్ పరంగా వేలన్సీ మారే విధానం: ప్రాతినిధ్య మూలకాలలో ఎడమ నుండి కుడికి వేలన్సీ 1 నుండి 4 వరకు పెరిగి మరల 1 వరకు తగ్గుతుంది.
3వ పీరియడ్ మూలకాల వేలన్సీలు :

ప్రశ్న 76.
కర్ణ సంబంధం అంటే ఏమిటి ? కర్ణ సంబంధం గల ఒక మూలకాల జంటను తెలపండి. అవి ఈ సంబంధాన్ని ఎందుకు చూపిస్తాయి ?
జవాబు:
ఇది రెండవ మరియు మూడవ పీరియడ్లకు సంబంధించినది. “ఆవర్తన పట్టికలో రెండో పీరియడ్లోని ఒక మూలకానికి, మూడో పీరియడ్లోని తర్వాత గ్రూపులోని రెండో మూలకానికి సారూప్య ధర్మాలుంటాయి. ఈ సంబంధాన్ని కర్ణ సంబంధం అంటారు.
ఉదా : (Li, Mg); (Be, Al); (B, Si)

ప్రశ్న 77.
లాంథనైడ్ సంకోచం అంటే ఏమిటి ? వాటి ఫలితాలు ఏమిటి ?
జవాబు:
లాంథనైడులలో ఎడమ నుండి కుడికి వాటి పరిమాణాలు నిలకడగా తగ్గుతూ వస్తాయి. పరిమాణంలో ఈ తగ్గుదలను, లాంథనైడ్ సంకోచమంటారు. Ce నుంచి Lu వరకు ఈ తగ్గుదల 0.2 ఉన్నది.
లాంథనైడులలో భేదాత్మక ఎలక్ట్రాన్లు (n – 2) f ఉపకక్ష్యలో ప్రవేశిస్తుంది. వితరణం చెందిన ఆకృతుల మూలంగా, f ఆర్బిటాళ్లు, కేంద్రకాకర్షణ నుండి వేలన్సీ ఎలక్ట్రాన్లకు తగు పరిరక్షణ కల్పించలేవు. ఆ కారణంగా కేంద్రక ఆకర్షణ వలన పరమాణు సైజులు ఎడమ నుండి కుడికి తగ్గుతాయి.
ఈ పరమాణు సైజు తగ్గుదల, లాంథనైడ్ పరమాణువుల (Ln) కన్నా వాటి +3 అయాన్ల (Ln3+) లో క్రమపద్ధతిలో ఉంటుంది.

ఫలితాలు :
- లాంథనైడ్ సంకోచం వలన మూలకాల ద్రస్థా, బా. స్థా, గట్టిదనం Ce నుండి Lu వరకు పెరుగుతాయి.
- 44 మరియు 5d శ్రేణులలోని గ్రూపుల మూలకాలలో అధిక సారూప్యతలు గోచరిస్తాయి. ఈ సారూప్యత, 3d మరియు 4d శ్రేణుల గ్రూపుల మూలకాలలో కన్పించదు. దీనికి కారణం, “లాంథనైడ్ సంకోచము”.
ఉదా : (Zr, Hf); (Nb, Ta); (Mo, W) మూలకాల జంటల సైజులు దాదాపు ఒకటే ఉంటాయి. కాబట్టి ఈ మూలకాల జంటల రసాయన ధర్మాలు కూడా ఒకే విధంగా ఉంటాయి. ఈ జంటలలో మొదటిది 4d మరియు రెండవది 5d మూలకము.
![]()
ప్రశ్న 78.
లిథియం ప్రథమ IE1 5.41 eν. Cl ఎలక్ట్రాన్ అఫినిటి -3.61eν
Li(g) + Cl(g) → \({L i^{+}}_{(g)}\) + \(\mathrm{Cl}^{-}(\mathrm{g})\) : ఈ చర్య ΔH ను KJ mol-1 లో లెక్కించండి.
జవాబు:

ప్రశ్న 79.
Cl + e → Cl– ప్రక్రియలో ఒక అవగాడ్రో సంఖ్యలోని పరమాణువులకు విడుదలయ్యే శక్తితో Cl → Cl+ + e– ప్రక్రియలో ఎన్ని Cl పరమాణువులను అయనీకరణం చెందించవచ్చు.
జవాబు:
వాయుస్థితిలోని ఒంటరి తటస్థ పరమాణువు ఎలక్ట్రాన్ను గ్రహించినప్పుడు విడుదలయ్యే శక్తి ఎలక్ట్రాన్ అఫినిటీ.
Cl + e– → \(\mathrm{Cl}^{-}(\mathrm{g})\) EA = 360 eV/atn
అవగాడ్రో సంఖ్యలో Cl పరమాణువులు ఉన్నప్పుడు విడుదలయ్యే శక్తి = 6.02 × 1023 × 3.60 = 21.6 × 1023 eV.
క్లోరిన్ అయనీకరణ శక్తి Cl → Cl+ + e–, IE = 13.0 eV
21.6 × 1023 eV లతో అయనీకరణం చెందించే క్లోరిన్ పరమాణువుల సంఖ్య.
= \(\frac{21.6 \times 10^{23}}{13}\) = 1.662 × 1023
ప్రశ్న 80.
Cl– ఎలక్ట్రాన్ అఫినిటీ 3.7ev. వాయుస్థితిలో 2 g. క్లోరిన్ పరమాణువులు పూర్తిగా Cl– అయాన్లుగా మారినప్పుడు KCal లలో ఎంత శక్తి విడుదల అగును ? (leV = 23.06 KCal mol-1)
జవాబు:
1eV = 23.06 KCal/mol
ఒక మోల్ క్లోరిన్ పరమాణువులు Cl– అయాన్లుగా మారినప్పుడు విడుదలయ్యే శక్తి = 3.7 × 23.06 KCal/mo/ అంటే 35.5గ్రాల Cl విడుదలచేసే శక్తి = 3.7 × 23.06 KCal/ml
2g క్లోరిన్ విడుదలచేసే శక్తి = \(\frac{2 \times 3.7 \times 23.06}{35.5}\) = 4.8069 KCal.
దీర్ఘ సమాధాన ప్రశ్నలు
ప్రశ్న 81.
మెండలీవ్ మూలకాల వర్గీకరణ గురించి రాయండి.
జవాబు:
మెండలీవ్ మరియు లోథర్ మేయర్లు మూలకాలను వాటి పరమాణు భారాల ఆధారంగా వర్గీకరించారు. మూలకాలను వాటి పరమాణు భారాల ఆరోహణ క్రమంలో అమర్చినప్పుడు మూలక ధర్మాలు ఆవర్తన మవుతాయని మెండలీవ్ చూపాడు.
మెండలీవ్ ఆవర్తన నియమం : “మూలకాల, వాటి సమ్మేళనాల భౌతిక, రసాయన ధర్మాలు వాటి వాటి పరమాణు భారాల ఆవర్తన ప్రమేయాలు”.
అప్పటి వరకు కనుగొన్న 65 మూలకాలను మెండలీవ్ తన ఆవర్తన పట్టికలో అమర్చాడు. మూలకాలను పట్టికలో అమర్చేటప్పుడు, మెండలీవ్ వాటి పరమాణుభారాలనే గాక వాటి రసాయన ధర్మాలను కూడా దృష్టిలో పెట్టుకున్నాడు.
ఆవర్తన నియమం వివరణ : మూలకాలను వాటి పరమాణు భారాల ఆరోహణ క్రమంలో వ్రాసినప్పుడు, సదృశమైన పోలికలు గల మూలకాలు, నిర్దిష్ట వ్యవధుల తర్వాత మరల మరల ఆవర్తనమవుతాయి. కాబట్టి ఈ అమరికకు ‘ఆవర్తన పట్టిక’ అని పేరు పెట్టారు. ప్రకృతిలో రోజులు, వారాలు, నెలలు, ఋతువులు, సంవత్సరాల మొ||నవి నిర్దిష్ట కాలవ్యవధుల తర్వాత ఆవర్తనం చెందడంతో, దీన్ని పోల్చవచ్చు.
మెండలీవ్ ఆవర్తన పట్టిక : మెండలీవ్ ప్రతి మూలకానికి ఒక సంఖ్యను గుర్తుగా ఇచ్చాడు. అది దాని పరమాణు సంఖ్య. మూలకాలను అడ్డశ్రేణులలోను, నిలువుగడుల్లోను అమర్చాడు. అడ్డశ్రేణులను ‘పీరియడ్’లని, నిలువుగళ్లను ‘గ్రూపు’లని మెండలీవ్ తెల్పినాడు. మెండలీవ్ యొక్క సవరింపబడ్డ సంక్షిప్త ఆవర్తన పట్టికలో 9 గ్రూపులు ఉన్నాయి. అవి, I నుండి VIII వరకు మరియు సున్నా (0) గ్రూపులు. మొదటి ఏడు గ్రూపులను A మరియు B అనే ఉపగ్రూపులుగా విభజించాడు. ఈ పట్టికలో 7 పీరియడ్లున్నాయి.
VIIIవ గ్రూపులో మూడు త్రికాలు (Triads, ట్రయడ్లు) ఉన్నాయి. అవి (Fe, Co, Ni); (Ru, Rh, Pd) మరియు (Os, Ir, Pt) పరివర్తన మూలకాలు.
మెండలీవ్ గుర్తించిన విషయాలు :
- మూలకాలను వాటి పరమాణు భారాల ఆరోహణక్రమంలో వ్రాసినప్పుడు, వాటి ధర్మాలలో ఆవర్తన ప్రదర్శిస్తాయి.
- a) ఒకే రకమైన ధర్మాలున్న మూలకాలకు దాదాపు సమాన పరమాణు భారాలుంటాయి.
ఉదా : Fe(56), CO(59), Ni(59)
OS (191), Lr (193), Pt (195)
(b) పరమాణు భారాలు స్థిరంగా పెరుగుతుంటాయి.
ఉదా : IA గ్రూపు మూలకాలలో K(39), Rb(85), CS (133) (తేడా సుమారు 47) - మూలకపు గ్రూపు సంఖ్య, ఆ మూలకపు వేలెన్సీని తెలుపుతుంది.
- అల్ప పరమాణు భారాలు గల మూలకాలన్నీ ప్రకృతిలో విరివిగా దొరుకుతాయి. ఉదా : H, C, O, N, Si, S మొ||నవి. వీటిని విలక్షణ మూలకాలంటారు. వీటికి పరమాణు భారాలు తక్కువగా ఉంటాయి.
- ఆసన్న పరమాణువుల పరమాణు ధర్మాల ఆధారంగా, ఒక మూలకపు సరియైన పరమాణు భారాన్ని లెక్క గట్టవచ్చు. ఆ విధంగా Be, ln, U ల పరమాణుభారాలను సవరించారు.
మెండలీవ్ ఆవర్తన పట్టిక విశిష్టతలు :
1) తర్వాత కాలంలో ఏర్పరచబడ్డ అనేక రకాల ఆవర్తన పట్టికలకు; మూలాధారం మెండలీవ్ ఆవర్తన పట్టికయే.
2) ఆసన్న మూలకాలు, వాటి సమ్మేళనాలను అధ్యయనం చేసి మెండలీవ్ కొన్ని తెలియని మూలకాల ధర్మాలు చెప్పాడు. మెండలీవ్ ఊహించిన ఆ మూలకాలు తర్వాత కనుక్కోబడ్డాయి. మెండలీవ్ ఊహించిన మూలకాల లక్షణాలు, కనుక్కోబడ్డ మూలకాల లక్షణాలు చాలా ఖచ్చితంగా సరిపోయాయి.
ఉదా : ఎకా బోరాన్ (సోడియం), ఎకా సిలికాన్ (జెర్మేనియం), ఎకా అల్యూమినియం (గాలియం) మొ||నవి.
3) మెండలీవ్ కాలానికి గ్రూపు “0” మూలకాలు తెలియవు. తర్వాత వాటిని కాలక్రమేణా కనుగొన్నారు. ఈ మూలకాలు మెండలీవ్ పట్టికలో సరియైన స్థానంలో అమరాయి.
4) ఆధునిక మెండలీవ్ ఆవర్తన పట్టికలో పరమాణుభారాల వరుసలు జతల మూలకాల్లో అపక్రమంలో ఉన్నాయి. అవి టెల్యూరియం – అయొడిన్, ఆర్గాన్ – పొటాషియం, కోబాల్టు – నికెల్, టెల్యూరియం – అయోడిన్ మరియు థోరియం – ప్రోటాక్టేనియంలు. ఈ జంటలలో మొదటి దానికన్నా రెండవ మూలకం పరమాణు భారం అధికము. వీటిని ‘అసంగత జంట’ అంటారు. కాని రసాయన ధర్మాలు మరియు పరమాణు సంఖ్యలను బట్టి చూస్తే, ఈ అమరిక సరియైనదేనని తెలుస్తుంది.
మెండలీవ్ ఆవర్తన పట్టిక అవధులు :
- కొన్ని మూలకాల స్థానాలు వాటి రసాయన ధర్మాలకు అనుగుణంగా లేవు.
ఉదా : నాణెలోహాలైన Cu, Ag, Au లను క్షారలోహాలైన K, Rb, CS లో కలిపి I గ్రూపులో ఉంచారు. నాణెలోహాలకు, క్షారలోహాలకు ధర్మాలలో చాలా భేదమున్నది. ఈ రెండు రకాల మూలకాలకు వేలన్సీ మాత్రం సమానంగా ఉన్నది (వేలన్సీ = 1). ఆ కారణం కావచ్చు. - విరళమృత్తిక (లాంథనైడ్)లను ఈ పట్టికలో ఒకే స్థానంలో ఉంచారు.
- హైడ్రోజన్ స్థానం సంతృప్తికరంగా లేదు. ఇది అటు క్షారలోహాలను (IA) ఇటు హేలోజన్ అలోహాలను (VIIA) పోలిన ధర్మాలు చూపుతుంది.
ప్రశ్న 82.
తెలియని మూలకం ధర్మాలను, దాని పక్కనున్న మూలకాల ధర్మాల అధ్యయనం వల్ల, నిర్దేశించవచ్చు – ఒక ఉదాహరణతొ సమర్థించండి.
జవాబు:
మూలకాలను, వాటి సమ్మేళనాలను అధ్యయనం చేసి, మెండలీవ్ కొన్ని తెలియని మూలకాల ధర్మాలను చెప్పగలిగాడు.. ఆవర్తన పట్టికను ఏర్పరచిననాటికి, సోడియం, గాలియం, జెర్మేనియం మొ॥ కొన్ని మూలకలు ఆవిష్కరింపబడలేదు. మెండలీవ్ ఆ మూలకాల ధర్మాలను ఊహించడమేగాక ఆ మూలకాలకు ఎకా బోరాన్, ఎకా అల్యూమినియం, ఎకా సిలికాన్ మొ॥ పేర్లు కూడా పెట్టాడు. పైన చెప్పిన మూడు మూలకాలు, మెండలీవ్ కాలంలోనే కనుక్కోబడ్డాయి. విశేషమేమంటే ప్రయోగాత్మకంగా కనుగొన్న ఆ మూలకాల ధర్మాలు, మెండలీవ్ ఊహించిన ధర్మాలు ఖచ్చితంగా సరిపోయాయి.
ఉదాహరణ : ఎకా అల్యూమినియం లేదా గాలియం.

ఇవి గాక మెండలీవ్ మరికొన్ని మూలకాలను ఊహించి, ధర్మాలు తెలిపాడు.
ప్రశ్న 83.
విస్తృత ఆవర్తన పట్టిక నిర్మాణాన్ని తెలపండి.
జవాబు:
మూలకానికి విలక్షణమైన ధర్మం పరమాణు సంఖ్యగాని పరమాణు భారం కాదని మోస్లే ప్రయోగాత్మకంగా నిర్ణయించారు. అనగా మూలక ధర్మాలు వాటి పరమాణు సంఖ్యతో మారుతాయి. అప్పుడు ఆవర్తన నియమాన్ని సవరించారు. “మూలకాల భౌతిక, రసాయన ధర్మాలు వాటి పరమాణు సంఖ్యల ఆవర్తన ప్రమేయాలు”. మూలకాల ధర్మాలు, పరమాణు సంఖ్య కన్నా, పరమాణువు ఎలక్ట్రాన్ నిర్మితిపై అధికంగా ఆధారపడతాయని తెలియడంతో, మరొక మారు ఆవర్తన సిద్ధాంతమును సవరించారు. నూతన ఆవర్తన నియమం ప్రకారం “మూలకాల భౌతిక రసాయన ధర్మాలు వాటి పరమాణువుల ఎలక్ట్రాన్ విన్యాసాల ఆవర్తన ప్రమేయాలు’. మూలకాల ఎలక్ట్రాన్ విన్యాసం ఆధారం చేసుకొని నీల్బోర్ విస్తృతావర్తన పట్టికను నిర్మించారు.
విస్తృత ఆవర్తన పట్టిక యొక్క ముఖ్యమైన లక్షణాలు :
- పరమాణు సంఖ్య ఆధారంగా ఈ పట్టిక తయారుచేయబడింది.
- మూలకాల ధర్మాలలోని పోలికలను, భేదాలను మరియు మార్పులను ఈ పట్టిక ప్రతిఫలిస్తుంది.
- ఈ పట్టికలోని విషయాలను గ్రహించడం, గుర్తుంచుకోవడం, తిరిగి తెలియజేయడం సులభము.
- పట్టికలోని నిలువు గళ్ళను గ్రూపులని, అడ్డ శ్రేణులను పీరియడ్లని పిలుస్తారు.
- ఈ పట్టికలో 7 పీరియడ్లున్నాయి. మొదటి పీరియడ్లో 2, రెండవ మరియు మూడవ పీరియడ్లలో 8 చొప్పున, నాల్గు మరియు ఐదవ పీరియడ్లలో 18 చొప్పున మూలకాలున్నాయి. ఆరవ పీరియడ్లో 36 ఉన్నాయి. ఏడవ పీరియడ్లో 19 ఉండి, అసంపూర్ణమైనది.
- 1వ పీరియడ్ : అతి పొట్టిది
2, 3 పీరియడ్లు : పొట్టివి
4, 5 పీరియడ్లు : పొడవైనవి.
6వ పీరియడ్ : అతి పొడవైనది
7వ పీరియడ్ : అసంపూర్ణము - ఈ పట్టికలో 18 గ్రూపులున్నాయి. అవి వరుసగా IA, IIA, IIIB, IVB, V B, VI B, VII B, VIII (దీనిలో 3), IB, IIB, IIIA, IV A, V A, VI A, VIIA మరియు ‘0’ గ్రూపులు.
- అన్ని A గ్రూపు లలోని మూలకాలను ప్రాతినిధ్య లేదా సాధారణ (normal) మూలకాలంటారు.
- అన్ని B గ్రూపు మూలకాలను పరివర్తన మూలకాలంటారు.
- పట్టిక కుడి చివరన ‘0’ గ్రూపులో జడవాయువులను ఉంచారు. వీటికి స్థిరమైన ఎలక్ట్రాన్ అష్టక నిర్మాణం ns2 np వేలన్సీ కక్ష్యలో ఉంటుంది. (Heకు 1s2)
- మెండలీవ్ ఆవర్తన పట్టికలోని పొట్టి పీరియడ్లను విడగొట్టినారు. పొడుగు పీరియడ్లలో మధ్యలో పరివర్తన మూలకాలను చేర్చి, పీరియడ్ను విస్తృతపరచారు.
- ప్రధాన పట్టిక నుండి వేరుగా, దిగువ భాగంలో, రెండు శ్రేణులలో లాంథనైడు మరియు ఆక్టినైడులనుంచారు.
- భేదపరచే ఎలక్ట్రాన్ స్థానాన్ని బట్టి, మూలకాలను నాల్గు బ్లాకులుగా విభజింపవచ్చు. అవి s, p, d, మరియు f బ్లాకులు. భేదపరచే ఎలక్ట్రానును s ఉపస్థాయిలో గల మూలకాలు S బ్లాకుకు, p ఉపస్థాయిలో గల మూలకాలు p బ్లాకుకు చెందుతాయి. ఇదే విధంగా మరియు నీ బ్లాకు మూలకాలు.
- అసంపూర్తిగా మరియు పూర్తిగా నిండిన ఎలక్ట్రాన్ కక్ష్యల ఆధారంగా, మూలకాలను రకాలుగా విభజింపవచ్చు.
నాల్గు
అవి –- మొదటి రకం మూలకాలు : జడవాయువులు – బాహ్యతమ కక్ష్య (n) నిండి ఉంటుంది.
- రెండవ రకం మూలకాలు : బాహ్యతమ కక్ష్య అసంపూర్ణంగా నిండి ఉంటుంది. దీనిలో S బ్లాకు మరియు ‘0’ గ్రూపు తప్ప మిగతా p బ్లాకు మూలకాలు ఉంటాయి. ఇవి ప్రాతినిధ్య మూలకాలు.
- మూడవ రకం మూలకాలు : బాహ్య రెండు కక్ష్యలు అనగా n మరియు (n – 1) కక్ష్యలు అసంపూర్ణంగా నిండి ఉంటాయి. ఇవి పరివర్తన మూలకాలు.
- నాల్గవ రకం మూలకాలు : వీనిలో బాహ్య మూడు కక్ష్యలు అనగా n, (n – 1) మరియు (n – 2) కక్ష్యలు అసంపూర్ణంగా నిండి ఉంటాయి. ఇవి అంతరపరివర్తన మూలకాలు.
- మూలకాల బాహ్యతమ కక్ష్య ఎలక్ట్రాన్ సాధారణ నిర్మితి :
s — బ్లాకు : ns1 – 2; p-బ్లాకు : ns2np1-6
d బ్లాకు : ns1 – 2 (n – 1) d1 – 10, f బ్లాకు (n – 2)f1 – 14 (n – 1) d0 – 1 ns2 - ఒక గ్రూపులోని మూలకాలలో వేలన్సీ ఎలక్ట్రాన్లు సమాన సంఖ్యలో ఉన్నందున అవి సమాన ధర్మాలు ప్రదర్శిస్తాయి.
- పీరియడ్లో ఎడమ నుండి కుడికి వెళ్ళేకొద్దీ, ఇంద్ర ధనస్సులో రంగులు మారినట్లు ధర్మాలు క్రమంగా మారుతూంటాయి.


![]()
ప్రశ్న 84.
కక్ష్యలోని ఉపశక్తి స్థాయిలలో పూర్తిగా నిండిన ఎలక్ట్రాన్ల సంఖ్యకు, పీరియడ్లో ఉండే మూలకాల అత్యధిక సంఖ్యకూ గల సంబంధాన్ని విశదీకరించండి.
జవాబు:
పీరియడ్ల నిర్మాణం :
a) 1వ పీరియడ్ (అతి సంక్షిప్తమైనది) : దీనిలో రెండు మూలకాలు 1H మరియు 2He మాత్రమే ఉన్నాయి. హైడ్రోజన్ ఒక విలక్షణ మూలకం. దీన్ని కొన్నిసార్లు పట్టిక పైభాగంలో విడిగా ఉంచుతారు. K కక్ష్య (n = 1) లో రెండు ఎలక్ట్రాన్లు మాత్రమే ఉండగలవు. అందువల్ల ఈ పీరియడ్లో రెండే మూలకాలున్నాయి.
b) 2వ పీరియడ్ (సంక్షిప్తమైనది) : దీనిలో 3Li నుండి 10Ne వరకు 8 మూలకాలుంటాయి.
Li పరమాణువులో K – కక్ష్య నుండి కొత్త కక్ష్య L లోకి ఒక ఎలక్ట్రాన్ ప్రవేశిస్తుంది. పీరియడ్లోని మిగతా మూలకాలలో అంటే Be నుండి Ne వరకు L కక్ష్య క్రమంగా నిండుతుంది. Ne లో K, L కక్ష్యలు పూర్తిగా నిండుతాయి.
ఆ విధంగా ఈ పీరియడ్ అంతమవుతుంది. ఈ మూలకాలలో, రెండవ శక్తి స్థాయి (L) క్రమంగా నిండి గరిష్ఠంగా 8 ఎలక్ట్రానులతో అంతమవుతుంది. కాబట్టి ఈ పీరియడ్లో 8 మూలకాలుంటాయి.
c) 3వ పీరియడ్ (సంక్షిప్తమైనది) : దీనిలో కూడా 11Na నుండి 18Ar వరకు 8 మూలకాలుంటాయి.
సోడియంలో M కక్ష్య ప్రారంభమవుతుంది. ఈ కక్ష్య ఆర్గాన్ వచ్చే వరకు క్రమంగా నిండుతుంది. అందువల్ల ఈ పీరియడ్లో 8 మూలకాలే ఉంటాయి.
ఆర్గాన్ తర్వాత, భేదపరిచే ఎలక్ట్రాన్ M కక్ష్యలోకి పోదు. దాని బదులు N కక్ష్య (అనగా 4వ కక్ష్య)లో ప్రవేశిస్తుంది. ఇది పొటాషియం (k) తో మొదలవుతుంది.
d) 4వ పీరియడ్ (విస్తృతమైనది) : దీనిలో 19K నుండి 36Kr వరకు 18 మూలకాలుంటాయి. పైన చెప్పినట్లు, Ar తర్వాత భేదపరచే ఎలక్ట్రాన్ M కక్ష్యలోకి వెళ్ళకుండా పొటాషియం (K) యొక్క N కక్ష్యలో ప్రవేశిస్తుంది.
![]()
తర్వాతి మూలకం Ca తో అదే కక్ష్య N లోకి భేదపరచే ఎలక్ట్రాన్ ప్రవేశిస్తుంది.
![]()
Ca తర్వాత, భేదపరచే ఎలక్ట్రాన్ లోపలి M కక్ష్యలో ప్రవేశించి, Sc (Z = 21) నుండి Zn (Z = 30) వరకు M కక్ష్య క్రమంగా నిండి మొత్తం 18 ఎలక్ట్రాన్లు కల్గి ఉంటుంది. Zn లో M కక్ష్య నిండుతుంది. Cr మరియు Cu లు మాత్రము Nth కక్ష్యలో ఒక్కొక్క ఎలక్ట్రానును మాత్రమే కల్గి ఉంటాయి. మిగతా అన్నింటిలో Nth కక్ష్యలో 2 ఎలక్ట్రాన్ల చొప్పున ఉంటాయి.
తర్వాత వచ్చే మూలకాలు Ga నుండి Kr వరకు N కక్ష్యలోకి ఎలక్ట్రాన్లు వచ్చి చేరుతాయి. 4వ పీరియడ్లో 4s, 3d, 4p, ఉపస్థాయిలు క్రమంగా నిండుతాయి. అందువల్ల ఈ పీరియడ్లో 18 మూలకాలుంటాయి.
e) 5వ పీరియడ్ (విస్తృతమైనది) : ఇది కూడా 4వ పీరియడ్ వలెనే ఎలక్ట్రాన్లతో క్రమంగా నిండుతుంది. దీనిలో Rb లో 5s ఎలక్ట్రాను మొదలవుతుంది. 5p ఉపకక్ష్య నిండే వరకు ఎలక్ట్రాన్లు చేరుతాయి. ఈ పీరియడ్లో 5s, 4d మరియు 5p ఉపస్థాయిలు క్రమంగా నిండుతాయి. కాబట్టి ఈ పీరియడ్లో Rb నుండి Xe వరకు మొత్తం 18 మూలకాలుంటాయి.
f) 6వ పీరియడ్ (అతి విస్తృతమైనది) : దీనిలో 6s, 4f, 5d మరియు 6p ఉపస్థాయిలు క్రమంగా నిండుతాయి. ఈ పీరియడ్లో 14 లాంథనైడ్లు కూడా కలసి ఉంటాయి. ఈ ఉపస్థాయిలన్నింటిని నింపగల ఎలక్ట్రాన్ల గరిష్ఠ సంఖ్య 32. కాబట్టి ఈ పీరియడ్లో 32 మూలకాలున్నాయి.
g) 7వ పీరియడ్ (అసంపూర్ణమైనది) : దీనిలో 14 ఆక్టినైడులు కలసి ఉంటాయి. వానితో సహా మొత్తం 20 మూలకాలు ఈ పీరియడ్లో ఉంటాయి.
ప్రశ్న 85.
s, p, d, f బ్లాక్ మూలకాలపై వ్యాసాన్ని రాయండి.
జవాబు:
మూలకాలను s, p, d, f బ్లాకులుగా వర్గీకరించడం: భేదపరచే ఎలక్ట్రాన్ పరమాణువులోని ఉపస్థాయిలోకి ప్రవేశించడం ఆధారంగా, మూలకాలను నాల్గు బ్లాకులుగా విభజింపవచ్చు. అవి s, p, d మరియు f బ్లాకు మూలకాలు.
s – బ్లాకు మూలకాలు : భేదపరచే ఎలక్ట్రాను ఉపస్థాయిలో గల మూలకాలు, S బ్లాకు మూలకాలు. ఈ మూలకాలలో S – ఉపస్థాయి పాక్షికంగా గాని, పూర్తిగా గాని ఎలక్ట్రానులతో నిండి ఉంటుంది. s ఆర్బిటాల్లో అత్యధికంగా రెండు ఎలక్ట్రాన్లు ఉండవచ్చు. అందువల్ల S బ్లాకులో రెండు గ్రూపులుంటాయి. అవి IA, IIA గ్రూపులు.
IA గ్రూపు : క్షారలోహాలు. బాహ్య ఎలక్ట్రాన్ విన్యాసం ns1.
IIA గ్రూపు : క్షారమృత్తిక లోహాలు. బాహ్య ఎలక్ట్రాన్ విన్యాసం ns2.
S – బ్లాకు మూలకాలు అన్నీ చాలా చురుకైన లోహాలు. అందువల్ల ప్రకృతిలో స్వేచ్ఛా స్థితిలో లభించవు. చర్యలలో ఇవి 1 లేదా 2 ఎలక్ట్రాన్లను కోల్పోయి Na+, Ca2+ వంటి అయాన్ల నేర్పరుస్తాయి. ఇవి అధిక ధన విద్యుదాత్మకత గల లోహాలు. లోహస్వభావం మరియు చర్యా శీలత, గ్రూపులో పరమాణు సంఖ్య పెరిగే కొద్దీ పెరుగుతాయి.
p – బ్లాకు మూలకాలు : వీనిలో p ఆర్బిటాల్ క్రమంగా నిండుతుంది. p ఉపస్థాయిలో అత్యధికంగా ఆరు ఎలక్ట్రానులుండవచ్చు. కాబట్టి దీనిలో ఆరు గ్రూపులున్నాయి. వీటి బాహ్య కక్ష్య ఎలక్ట్రాన్ విన్యాసం ns2 npx (x = 1 నుండి 6 వరకు)
p బ్లాకులో లోహాలు, అర్ధలోహాలు, అలోహాలు ఉంటాయి. లోహాల చురుకుదనం S బ్లాకు కన్నా తక్కువ. S మరియు p బ్లాకు (0 గ్రూపుమినహా) మూలకాలను కలిపి ‘ప్రాతినిధ్య మూలకాలు’ లేదా ప్రధాన గ్రూపు మూలకాలంటారు. p బ్లాకులో ‘0’ గ్రూపులో జడ మూలకాలుంటాయి. వీటి వేలెన్సీ 0. VII గ్రూపులో హాలోజన్లు చాలా చురుకైనవి. VI గ్రూపు మూలకాలను చాల్కోజన్ లంటారు. ఇవి కూడా చురుకైనవే. ఈ గ్రూపులలో పై నుండి క్రిందకు అలోహ ధర్మం తగ్గి లోహ ధర్మం పెరుగుతుంది.
d – బ్లాకు మూలకాలు : వీటిలో ‘d’ ఆర్బిటాల్ క్రమంగా నిండుతుంది. ఇవి s మరియు p బ్లాకుల మధ్యన వారధివలె ఉంటాయి. ఇవన్నీ లోహాలే. అంత చురుకైనవి కావు. వీటి బాహ్య విన్యాసం (n – 1) d1 – 10 ns,sup>1 – 2 గా ఉంటుంది. ఇవి 3d, 4d, 5d, 6d అనే నాల్గు శ్రేణులలో ఉంటాయి. 6d శ్రేణి ఆక్టేనియం (Ac) తో మొదలై అసంపూర్ణంగా ఉంటుంది. ప్రతిశ్రేణిలోను 10 చొప్పున మూలకాలుంటాయి. 3d – శ్రేణిలో Sc నుండి Zn వరకు, 4d – శ్రేణిలో Y నుండి Cd వరకు మరియు 5d – శ్రేణిలో La, Hf ల నుండి Hg వరకు ఉంటాయి.

ఈ బ్లాకు మూలకాల ధర్మాలు విశిష్టంగా ఉంటాయి. పెక్కు లోహాలు కాని అయాన్లు గాని రంగు కల్గి ఉంటాయి, అనేక ఆక్సీకరణ స్థితులు కల్గి ఉంటాయి మరియు సంక్లిష్ట సమ్మేళనాల నేర్పరుస్తాయి. ఇవి ఉత్ప్రేరకాలుగా ఉపయోగపడతాయి. మిశ్రలోహాలుగా బాగా ఉపయోగపడతాయి.
f – బ్లాకు మూలకాలు : ఇవి ఆవర్తన పట్టిక క్రింద రెండు వరుసలలో ఉన్నాయి. అవి : 4f శ్రేణి లేదా లాంథనైడ్లు (Ce నుండి Lu వరకు) మరియు 51 శ్రేణి లేదా ఆక్టినైట్లు (Th నుండి Lw వరకు).
ప్రతి వరుసలో 14 మూలకాలుంటాయి. ఇవన్నీ లోహాలే. వీటి బాహ్య సాధారణ విన్యాసం, (n – 2)f1 – 14 (n – 1). d0 – 1 ns2. ఈ మూలకాలు రంగుగల అయాన్ల నేర్పరుస్తాయి, పారా అయస్కాంత ధర్మం కల్గి ఉంటాయి.
ప్రశ్న 86.
మూలకాల వర్గీకరణలో మూలకాల ఎలక్ట్రాన్ విన్యాసానికి, వాటి ధర్మాలకు గల సంబంధాన్ని తెలపండి.
జవాబు:
మూలకాలను వాటి లక్షణాల ప్రాతిపదిక మీద, వాటి ఎలక్ట్రాన్ విన్యాసం ఆధారంగా నాల్గు రకాలుగా విభజించారు.
అవి:
I ఉత్కృష్ట వాయు మూలకాలు
II ప్రాతినిథ్య మూలకాలు
III పరివర్తన మూలకాలు
IV అంతర్ పరివర్తన మూలకాలు
I. ఉత్కృష్ట వాయు మూలకాలు : ఇవి ‘0’ గ్రూపు మూలకాలు. వీటిని ‘విరళవాయువులు’ అని కూడా అంటారు. ఇవి He, Ne, Ar, Kr, Xe, Rn. He(1s2) తప్ప మిగతా మూలకాల బాహ్య సాధారణ ఎలక్ట్రాన్ విన్యాసం ns2 np6. వీటి జడత్వానికి కారణం, బాహ్యతమ కక్ష్యలో 8 ఎలక్ట్రానులుండటమే. He కు మాత్రం K కక్ష్య నిండినందువల్ల జడత్వం వచ్చింది. రేడాన్, రేడియోథార్మిక మూలకము.
II. ప్రాతినిథ్య మూలకాలు : ‘0’ గ్రూపు మూలకాలు గాక, మిగతా s మరియు p బ్లాకు మూలకాలు ఈ రకానికి చెందినవి. వీటి బాహ్యకక్ష్య విన్యాసం.ns1 – 2 np1 – 5 బ్లాకు మూలకాలన్నీ చురుకైన లోహాలు. ఇవి రసాయన చర్యలో ఎలక్ట్రాన్లను కోల్పోయి ధన అయానుల నేర్పరుస్తాయి. ఉదా : Na+, Ca2+. p బ్లాకులో లోహాలు, అర్థలోహాలు మరియు అలోహాలుంటాయి. ఇవి అయానిక మరియు సమయోజనీయ సమ్మేళనాల నేర్పరుస్తాయి. p బ్లాకులోని గ్రూపులలో పై నుండి క్రిందకు అలోహ ధర్మం తగ్గి లోహ ధర్మం పెరుగుతుంది. s – బ్లాకు మూలకాలలో పై నుండి క్రిందకు లోహధర్మం పెరుగుతుంది.
ఈ మూలకాలు చర్యలలో తరచుగా వస్తుంటాయి. కాబట్టి వీటిని ప్రాతినిధ్య మూలకాలని పిలిచారు.
III. పరివర్తన మూలకాలు : ఇవి s మరియు p బ్లాకుల మధ్యలో వంతెనవలె ఉంటాయి. ఈ మూలకాలేర్పరచే సమ్మేళనాలలో, అయానిక నుండి కోవెలంట్కు బంధ స్వభావాలు మారడం గమనిస్తాము. వీని బాహ్య ఎలక్ట్రాన్ విన్యాసం (n – 1) d1 – 10 ns1 – 2 గా ఉంటుంది. ఈ మూలకాలు ఒక ప్రత్యేకతను గల్గి ఉంటాయి. దానికి కారణాలు.
- అసంపూర్తిగా నిండిన d ఆర్బిటాళ్లు
- అధిక కేంద్రక ఆవేశం
- పరమాణు అల్పసైజు
పరివర్తన మూలకాల అభిలాక్షణిక ధర్మాలు :
- ఇవన్నీ గట్టి, భారీ లోహాలు
- వీని ద్ర.భ, బా.స్థా., సాంద్రత ఎక్కువ
- మంచి ఉష్ణ, విద్యుద్వాహకాలు
- ఒకటి కన్నా ఎక్కువ ఆక్సీకరణ స్థితులు కల్గి ఉంటాయి.
- ఈ మూలకాలు, వాటి సమ్మేళనాలు రసాయన చర్యల్లో మంచి ఉత్ప్రేరకాలుగా పనిచేస్తాయి.
- వీటి ఆర్బిటాళ్లు సాధారణంగా పారా అయస్కాంత ధర్మాన్ని చూపుతాయి.
- ఇవి మిశ్రలోహాలనిస్తాయి.
IV) అంతర్ పరివర్తన మూలకాలు : వీటి సాధారణ బాహ్య విన్యాసం (n – 2) f1 – 14 (n – 1) d0 – 1 ns2. కాబట్టి వీటిని కూడా d బ్లాకు మూలకాలతో చేర్చుతారు (d ఆర్బిటాల్ అసంపూర్ణం). కాని భేదాత్మక ఎలక్ట్రాను (n – 2)f ఉపస్థాయిలో ప్రవేశించడం వల్ల వీటిని f బ్లాకు మూలకాలంటారు. వీటి సాధారణ ఆక్సీకరణ స్థితి + 3.
అంతర్ పరివర్తన మూలకాలన్నీ లోహాలే. వీటిలో రెండు శ్రేణులున్నాయి అవి :
లాంథనైడులు – సీరియమ్ నుండి లుటీషియం వరకు. వీనిలో 4f ఆర్బిటాళ్ళు నిండుతాయి. ఇవి 14 మూలకాలు.
అక్టినైడులు – థోరియం నుండి లారెన్షియమ్ వరకు. వీనిలో 51 ఆర్బిటాళ్లు నిండుతాయి. ఇవి 14 మూలకాలు. Th, U వంటి కొన్ని మూలకాలు మినహాయిస్తే ఆక్షినైడులన్నీ కృత్రిమంగా తయారైనవే. ఇవన్నీ రేడియోధార్మిక మూలకాలు.
ప్రశ్న 87.
ఆవర్తన ధర్మమనగా నేమి ? కింది ధర్మాలు గ్రూప్ , పీరియడ్లో ఏ విధంగా మారతాయి ? విశదీకరించండి.
(a) పరమాణు వ్యాసార్థం
(b) ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ
జవాబు:
ఆవర్తన ధర్మం : ఆవర్తన పట్టికలో మూలకాల ధర్మాలు ఎలక్ట్రానిక్ విన్యాసంతో బాటు క్రమంగా మారుతాయి. ఈ మార్పుల సరళి క్రమ వ్యవధుల్లో పునరావృతమవుతుంది. ఇలా ఒక ధర్మం పునరావృతమవడాన్ని ‘ఆవర్తనం’ అంటారు. పునరావృతమయే ధర్మాన్ని ‘ఆవృత ధర్మం’ అంటారు.
పరమాణు వ్యాసార్థం : ఒక గ్రూపులో పైనుండి క్రిందికి వచ్చిన కొద్దీ, పరమాణు వ్యాసార్ధం పెరుగుతుంటుంది. కారణం గ్రూపులో క్రిందికి వచ్చిన కొద్దీ వేలన్సీ ఎలక్ట్రాన్లు కొత్త కక్ష్యలో ప్రవేశిస్తాయి. కేంద్రక ఆవేశం పెరిగినా కూడా, ఈ వేలన్సీ ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ అధికంగా ఉండనందున కక్ష్యలు దూరంగా జరుగుతాయి. అప్పుడు పరమాణు సైజు పెరుగుతుంది.
ఒక పీరియడ్లో ఎడమ నుండి కుడికి వెళ్ళిన కొద్దీ పరమాణు సైజు తగ్గుతుంది. కారణం, భేదాత్మక ఎలక్ట్రాన్ అదే కక్ష్యలోకి ప్రవేశిస్తుంది. కేంద్రక ఆవేశం కూడా పెరగడం వల్ల, ఈ కక్ష్యపై కేంద్రక ఆకర్షణ పెరుగుతుంది. దాని వల్ల కక్ష్యల సైజు తగ్గి పరమాణు సైజు తగ్గుతుంది.
ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ : గ్రూపులో పైనుంచి క్రిందికి పోయే కొద్దీ పరమాణు పరిమాణం పెరగడం వల్ల ఎలక్ట్రాన్ అఫినిటీ విలువలు తగ్గుతాయి.
పీరియడ్లో ఎడమ నుంచి కుడికి పోయే కొద్దీ పరమాణు పరిమాణం తగ్గుతుంది. మూలక స్వభావం లోహం నుంచి ఆలోహానికి మారుతుంది. దీని ఫలితంగా ఎలక్ట్రాన్లపై అపేక్ష పెరుగుతుంది. అంటే ఎలక్ట్రాన్ అఫినిటీ పెరుగుతుంది.
ప్రశ్న 88.
ఆవర్తన ధర్మం అంటే ఏమిటి ? కింది ధర్మాలు గ్రూప్లో, పీరియడ్లో ఎట్లా మారతాయి ? విశదీకరించండి.
a) IE
b) EN
జవాబు:
మూలకాలను వాటి ఎలక్ట్రాన్ విన్యాసాల ఆరోహణ క్రమంలో అమర్చితే సారూప్య ధర్మాలుగల మూలకాలు పునరావృతం అవుతాయి. నిర్ధిష్ట వ్యవధిలో పునరావృతమయ్యే ధర్మాలను ఆవర్తన ధర్మాలు అంటారు. పునరావృతమయ్యే ధర్మాన్ని ‘ఆవృత ధర్మం’ అంటారు.
a) IE. అయనీకరణ శక్తి : ఒక గ్రూపులో అయనీకరణ శక్తి పై నుండి క్రింది మూలకానికి తగ్గుతుంది. పరమాణు పరిమాణం పెరగడమే దీనికి కారణం.
ఒక’పీరియడ్లో అయనీకరణ శక్తి ఎడమ నుంచి కుడి మూలకానికి పెరుగుతుంది. పరమాణు పరిమాణం తగ్గడమే దీనికి కారణం.
b) EN. ఋణవిద్యుదాత్మకత : ఒక గ్రూపులో పై నుంచి క్రిందకు పోయే కొలదీ ఋణ విద్యుదాత్మకత తగ్గుతుంది. పరమాణు పరిమాణం పెరగడం వల్ల కేంద్రకానికి ఎలక్ట్రానును ఆకర్షించే శక్తి తగ్గుతుంది. అనగా ఋణ విద్యుదాత్మకత తగ్గుతుంది.
ఒక పీరియడ్లో ఎడమ నుంచి కుడికి ఋణ విద్యుదాత్మకత పెరుగుతుంది. పరమాణు పరిమాణం తగ్గడంవల్ల ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ పెరుగుతుంది. అంటే ఋణ విద్యుదాత్మకత పెరుగుతుంది.
ప్రశ్న 89.
a) పరమాణు వ్యాసార్ధం
b) లోహ వ్యాసార్ధం
c) సంయోజక వ్యాసార్ధంల గురించి రాయండి.
జవాబు:
a) పరమాణు (స్ఫటిక) వ్యాసార్ధం : లోహ స్ఫటికంలో రెండు ఆసన్న లోహ పరమాణు కేంద్రకాలు మధ్య బిందువుల మధ్య దూరంలో సగాన్ని పరమాణు (స్ఫటిక) వ్యాసార్ధం అంటారు.
ఉదా : రెండు సోడియం పరమాణు కేంద్రకాల మధ్య దూరం = 3.72 Å
∴ సోడియం పరమాణు వ్యాసార్ధం = \(\frac{1.98}{2}\) = 1.86 Å
b) లోహ (వాన్డర్వాల్) వ్యాసార్ధం : అతి సన్నిహితంగా వున్న భిన్న అణువుల్లోని రెండు పరమాణువుల కేంద్రకాల మధ్య దూరంలో సగాన్ని లోహ (వాన్గార్వాల్స్) వ్యాసార్థం అంటారు.
భిన్న అణువుల మధ్య వాన్ డర్వాల్ ఆకర్షణ బలాలున్నపుడు, ఆ అణువులు దగ్గరవుతాయి. కాని వాని మధ్య రసాయన బంధం ఉండదు. ఉదా : భిన్న క్లోరిన్ అణువుల్లోని ఆసన్న పరమాణువుల కనిష్ఠ దూరం 3.6 A. కాబట్టి క్లోరిన్ వాన్ డర్వాల్స్ వ్యాసార్ధం \(\frac{3.6}{2}\) = 1.8 À అవుతుంది. రసాయన బంధం కన్నా వానర్వాల్ ఆకర్షణలు బలహీనమైనందున అణువుల మధ్య దూరం ఎక్కువ, రసాయనిక బంధం కన్నా వాన్ డర్వాల్స్ వ్యాసార్ధం దాదాపు 40% అధికంగా ఉంటుంది.
c) సమయోజనీయ (కోవలెంట్) వ్యాసార్ధం : సజాతీయ పరమాణువులు గల అణువులో కోవలంట్ బంధంతో కలపబడిన రెండు పరమాణు కేంద్రకాల మధ్య దూరంలో సగాన్ని సమయోజనీయ (‘కోవలంట్) వ్యాసార్ధం అంటారు. ఉదా : క్లోరిన్ అణువులో పరమాణు కేంద్రకాల మధ్య దూరం 1.98À. ఇది బంధ దైర్ఘ్యం. కాబట్టి

క్లోరిన్ కోవలంట్ వ్యాసార్థం, \(\frac{1.98}{2}\) = 0.99 A
ఈ వ్యాసార్థాన్ని సాధారణంగా అలోహాలకు వాడుతారు.
ప్రశ్న 90.
IE1, IE2 లను నిర్వచించండి. ఏదైనా పరమాణువుకు IE2 > IE1 గా ఎందుకు ఉంటుంది ? ఒక మూలకపు IE ని ప్రభావితం చేసే అంశాలను చర్చించండి. (March 2013)
జవాబు:
అయనీకరణ శక్తి : “స్వేచ్ఛా స్థితిలో ఉండే వాయు పరమాణువు నుంచి అత్యంత బలహీనంగా బంధితమైన ఎలక్ట్రాను విడదీసి వాయు స్థితిలో అయాను ఏర్పరచడానికి అవసరమైన కనీస శక్తిని అయనీకరణ శక్తి” అంటారు.
దీన్ని ఒకటవ అయనీకరణ శక్తి అంటారు.
![]()
“ఏకధనావేశిత అయాన్ నుంచి రెండవ ఎలక్ట్రాన్ ను తీసివేయడానికి కావల్సిన కనీస శక్తిని రెండో అయొనైజేషన్ శక్తి (I2) అంటారు.
![]()
I2 >I1 కు కారణం : పరమాణువు నుంచి ఒక ఎలక్ట్రాన్ ను తీసివేస్తే ఏర్పడే ఏక ధనావేశిత అయానులో తటస్థ పరమాణువులో కన్నా అధిక ప్రాభావిక కేంద్రక ఆవేశం ఉంటుంది. దీనివల్ల ఎలక్ట్రాన్ల మధ్య వికర్షణలు తగ్గుతాయి. అదే సమయంలో బాహ్య కక్ష్యలలోని ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ పెరుగుతుంది. దీని ఫలితంగా ఏక ధనావేశిక అయాన్ నుంచి ఒక ఎలక్ట్రాన్ ను తీసివేయడానికి అధిక శక్తి అవసరమవుతుంది. కాబట్టి రెండవ అయనీకరణ శక్తి (I2) మొదటి అయనీకరణ శక్తి (I1) కన్నా ఎక్కువగా ఉంటుంది.
మూలకాల IP విలువలను ప్రభావితం చేసే అంశాలలో మూడు అంశాలు :
- పరమాణు వ్యాసార్ధం
- కేంద్రక ఆవేశం
- బాహ్య ఎలక్ట్రాన్లపై రక్షక ప్రభావం.
1) పరమాణు వ్యాసార్ధం : పరమాణు వ్యాసార్ధం పెరిగే కొద్దీ వేలెన్సీ ఎలక్ట్రాన్లు కేంద్రకం నుంచి దూరం అవుతాయి. కాబట్టి వాటిపై కేంద్రక ఆకర్షణ తగ్గుతుంది. అందువలన ఎలక్ట్రాన్లను తొలగించడానికి తక్కువ శక్తి సరిపోతుంది. అనగా,అయనీకరణ శక్తి తగ్గుతుంది. గ్రూపులోని మూలకాలకు పై నుండి క్రిందకు పరమాణు సైజు పెరిగినందున, IP విలువ తగ్గుతుంది.
I.P. ∝ \(\frac{1}{r}\)
అదే విధంగా పరమాణు సైజు తగ్గితే IP విలువ పెరుగుతుంది.
2) కేంద్రక ఆవేశం : ఎలక్ట్రాన్ కక్ష్యల సంఖ్య స్థిరంగా ఉండి కేంద్రకావేశం పెరిగినపుడు బాహ్య ఎలక్ట్రాన్లను కేంద్రకం ఎక్కువ బలంగా ఆకర్షిస్తుంది. దీనివల్ల బాహ్య ఎలక్ట్రానును తొలగించడానికి అధిక శక్తి అవసరము. అనగా IP విలువ అధికమవుతుంది.
I.P ∝ Z
3) బాహ్య ఎలక్ట్రాన్లపై రక్షక ప్రభావం : వేలన్సీ కక్ష్యకు, కేంద్రకానికి మధ్య గల కక్ష్యలలోని ఎలక్ట్రాన్లు కేంద్రకావేశాన్ని కొంత వరకు తటస్థీకరించడం వల్ల, బాహ్య కక్ష్యలోని ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ తగ్గుతుంది. అంతర్ కక్ష్యలలోని ఎలక్ట్రాన్లు బాహ్య కక్ష్యలోని ఎలక్ట్రాన్లకు – కేంద్రకానికి మధ్య గల ఆకర్షణపై కనబరచే ఈ ప్రభావాన్ని ‘పరిరక్షక ప్రభావం’ అంటారు. ఈ ప్రభావం పెరిగితే, అనగా అంతర్ కక్ష్యల సంఖ్య పెరిగే కొద్దీ అయొనైజేషన్ శక్తి తగ్గుతుంది.

ఆర్బిటాల్లోని ఎలక్ట్రాన్ల పరిరక్షక దక్షత అవరోహణ క్రమం s > p > d>f గా ఉంటుంది.
ప్రశ్న 91.
క్రింది చెప్పిన లక్షణాలు 1వ గ్రూపులోను, IIIవ పీరియడ్లోను ఎట్లా మారతాయో ఉదాహరణతో వివరించండి.
a) మూలకాల ఆక్సైడ్ స్వభావం
b) మూలకాల లోహ, అలోహ స్వభావాలు
c) అయనీకరణ శక్తి.
జవాబు:
a) మూలకాల ఆక్సైడ్ స్వభావం : IA గ్రూపు మూలకాలు క్షార మూలకాలు. వాటి ఆక్సైడ్లు (M2O) క్షార ప్రవృత్తి కల్గి ఉంటాయి. ఉదా : Li2O, Na2O, K2O. Li2O చాలా బలహీన క్షారధర్మం కలది . CS2O (సాధారణంగా ఏర్పడదు) చాలా బలమైన క్షార ధర్మం కలది.
క్షార ఆక్సైడ్లు నీటిలో కరిగి క్షారాన్నిస్తాయి.
ఉదా : Na2O + H2O → 2NaOH
IA గ్రూపులో, క్షార ఆక్సైడ్ స్వభావం, పై నుండి క్రిందకు పెరుగుతుంది.
3వ పీరియడ్లో ఎడమ నుండి కుడికి వెళ్తే, ఆక్సైడ్ స్వభావం క్షార స్వభావం నుంచి ఆమ్ల స్వభావానికి క్రమంగా మారుతుంది.

ఈ విధంగానే హైడ్రాక్సైడుల స్వభావం కూడా మారుతుంది.
b) మూలకాల లోహ, అలోహ స్వభావాలు : ఎలక్ట్రాన్ను వదలుకొని ధన అయాన్గా మారే మూలకాన్ని లోహమంటారు. ఎలక్ట్రాన్ను పొంది ఋణ అయానుగా మారే మూలకాన్ని అలోహమంటారు.
IA గ్రూపులో క్షారలోహాలు లోహప్రవృత్తిని అధికంగా చూపుతాయి. చర్యలలో ఇవి ధన అయానులుగా మారుతాయి. ఈ గ్రూపులో పై నుండి క్రిందకు పెరిగే కొద్దీ లోహ స్వభావం పెరుగుతుంది. Li కన్నా Cs అతి చురుకైన లోహము.
3వ పీరియడ్లో Na నుండి CI కు వెళ్ళేకొద్దీ లోహ స్వభావం తగ్గి అలోహ స్వభావం పెరుగుతుంది. Na కు అత్యధిక లోహ స్వభావం ఉన్నది. మధ్యలోని ALకు కొంత అలోహ స్వభావం ఉన్నది. తర్వాతి Si అలోహము. చివరగా ఉన్న Cl బలమైన అలోహము.
c) అయనీకరణశక్తి : IA గ్రూపులో పై నుండి క్రిందకు వెళ్ళే కొద్దీ పరమాణు సైజు పెరుగుతుంది. ఆ కారణం వల్ల అయనీకరణ శక్తి తగ్గుతుంది. మొదటి మూలకం Li కు అత్యధిక ‘I1 విలువ (I1 = 520 KJ/mol) ఉండగా దాదాపు చివరి మూలకం Cs కు అత్యల్ప I1 విలువ (I1 = 375 KJmol-1) ఉన్నది.
3వ పీరియడ్లో Na నుండి CI కు పరమాణు సైజు తగ్గినందువల్ల అయనీకరణ శక్తి పెరుగుతుంది. మొదటగల లోహాలకు తక్కువగాను చివర గల అలోహాలకు ఎక్కువగాను IP విలువలుంటాయి. (I1 : Na = 5.14 eV; Cl = 13 eV)
ప్రశ్న92.
అయొనైజేషన్ ఎంథాల్పీని ప్రభావితం చేసే వివిధ అంశాలపై వ్యాసం వ్రాయండి.
జవాబు:
ఒక పరమాణువు యొక్క అయనీకరణ శక్మం క్రింది అంశాలపై ఆధారపడుతుంది.
1. పరమాణు వ్యాసార్ధం
2. కేంద్రక ఆవేశం
3. బాహ్య ఎలక్ట్రాన్లపై రక్షణ ప్రభావం
4. వేలన్సీ ఎలక్ట్రాన్ల ఆర్బిటాల్లు చొచ్చుకొనిపోయే విస్తృతి
5. ఉపకక్ష్యల స్వభావం అవి సగం లేదా పూర్తిగా ఎలక్ట్రాన్లతో నిండి ఉండటం లేదా ఉండకపోవడం.
1) పరమాణు వ్యాసార్ధం : పరమాణు వ్యాసార్ధం పెరిగే కొద్దీ వేలన్సీ ఎలక్ట్రాన్లు కేంద్రకం నుంచి దూరం అవుతాయి. కాబట్టి వాటిపై కేంద్రక ఆకర్షణ తగ్గుతుంది. అందువలన ఎలక్ట్రాన్లను తొలగించడానికి తక్కువ శక్తి సరిపోతుంది. అనగా అయనీకరణ శక్తి తగ్గుతుంది. గ్రూపులోని మూలకాలకు పై నుండి క్రిందకు పరమాణు సైజు పెరిగినందున, IP విలువ తగ్గుతుంది.
I.P ∝ \(\frac{1}{r}\)
అదే విధంగా పరమాణు సైజు తగ్గితే IP విలువ, పెరుగుతుంది.
2) కేంద్రక ఆవేశం : ఎలక్ట్రాన్ కక్ష్యల సంఖ్య స్థిరంగా ఉండి కేంద్రకావేశం పెరిగినప్పుడు బాహ్య ఎలక్ట్రాన్లను కేంద్రకం ఎక్కువ బలంగా ఆకర్షిస్తుంది. దీనివల్ల బాహ్య ఎలక్ట్రాను తొలగించడానికి అధిక శక్తి అవసరము. అనగా IP విలువ అధికమవుతుంది. అంటే కేంద్రక ఆవేశం పెరిగే కొలది IP పెరుగుతుంది. ‘
I.P ∝ Z
3) బాహ్య ఎలక్ట్రాన్లపై రక్షక ప్రభావం : వేలన్సీ కక్ష్యకు, కేంద్రకానికి మధ్య గల కక్ష్యలలోని ఎలక్ట్రాన్లు కేంద్రకావేశాన్ని కొంత వరకు తటస్థీకరించడం వల్ల, బాహ్య కక్ష్యలోని ఎలక్ట్రాన్లపై కేంద్రక ఆకర్షణ తగ్గుతుంది. అంతర్ కక్ష్యలలోని ఎలక్ట్రాన్లు బాహ్య కక్ష్యలోని ఎలక్ట్రానులకు – కేంద్రకానికి మధ్య గల ఆకర్షణపై కనబరచే ఈ ప్రభావాన్ని ‘పరిరక్షక ప్రభావం’ అంటారు. ఈ ప్రభావం పెరిగితే, అనగా అంతర్ కక్ష్యల సంఖ్య పెరిగే, కొద్దీ అయొనైజేషన్ శక్తి తగ్గుతుంది.

ఆర్బిటాల్లోని ఎలక్ట్రాన్ల పరిరక్షక దక్షత అవరోహణ క్రమం s > p > d > f గా ఉంటుంది.
4) వేలన్సీ ఎలక్ట్రాన్ల ఆర్బిటాల్లు చొచ్చుకొనిపోయే విస్తృతి : ఒకే కక్ష్యకు చెందిన ఆర్బిటాళ్లు కేంద్రకం వైపుకు చొచ్చుకుపోయే క్రమము s > p > d > f గా ఉంటుంది. అనగా గోళాకార సౌష్ఠవం గల S ఆర్బిటాల్ అత్యధికంగాను, డంబెల్ ఆకారం గల P ఆర్బిటాల్ తక్కువగాను వితరణ చెందిన ఆకృతులు గల d మరియు f ఆర్బిటాళ్లు అతి తక్కువగాను కేంద్రకం వైపు చొచ్చుకుపోతాయి. ఈ చొచ్చుకుపోయే విస్తృతిని బట్టి ఆ ఆర్బిటాళ్లపై కేంద్రక ఆకర్షణ ప్రభావం ఉంటుంది. అయొనైజేషన్ పొటెన్షియల్ విలువలు ఆర్బిటాళ్లు చొచ్చుకుపోయే విస్తృతుల క్రమంలోనే ఉంటాయి. s > p > d > f. అనగా IP విలువ s – ఎలక్ట్రాన్కు అధికంగాను, f ఎలక్ట్రాన్కు అల్పంగాను ఉంటాయి.
5) పూర్తిగా నిండిన లేదా సగం నిండిన ఉపకర్పరాలు ఉండటం : సగం లేదా పూర్తిగా నిండిన ఉపశక్తి స్థాయిలు పరమాణువుకు అధిక స్థిరత్వాన్ని ఇస్తాయి. అటువంటి పరమాణువుల నుంచి ఎలక్ట్రాను వేరుచెయ్యడానికి అధిక శక్తి కావాలి. కాబట్టి వాటికి అయనీకరణ శక్తులు అధికంగా ఉంటాయి.
ప్రశ్న 93.
ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీని నిర్వచించండి. గ్రూప్ , పీరియడ్లో అది ఎలా మారుతుంది ? గ్రూప్ తర్వాత మూలకం కంటే O, F ల ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ ఎందుకు తక్కువ రుణాత్మకంగా ఉంటుంది ?
జవాబు:
వాయు స్థితిలోని తటస్థ పరమాణువును రుణాత్మక అయానుగా మార్చడానికి ఎలక్ట్రాన్ను కలిపే ప్రక్రియలో జరిగే ఎంథాల్పీలోని మార్పును ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ అంటారు. పరమాణువు ఎలక్ట్రాను గ్రహించి ఆనయానుగా మారే సామర్థ్యాన్ని ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ తెలియజేస్తుంది.
![]()
గ్రూపులో మార్పు : గ్రూపు మూలకాలలో ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ పై నుంచి కిందకి తగ్గుతుంది. ఎందుకంటే పరమాణు పరిమాణం పెరగడంవల్ల చేరే ఎలక్ట్రాన్ కేంద్రకానికి దూరంగా ఉంటుంది. అయినప్పటికీ తర్వాత ఉండే మూలకాల కంటె O, F ల ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ తక్కువ రుణాత్మకంగా ఉంది. O, F లకు ఎలక్ట్రాన్ చేర్చినపుడు చేరే ఎలక్ట్రాన్లు N = 2 క్వాంటమ్ స్థాయిలోకి వెళ్తుంది. అప్పటికే ఆ స్థాయిలో ఉన్న ఇతర ఎలక్ట్రాన్లతో ప్రాముఖ్యమైన వికర్షణకు లోనౌతుంది. అందువల్ల ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ తక్కువ రుణాత్మకంగా ఉంటుంది.
పీరియడ్లో మార్పు : పీరియడ్లో పరమాణు సంఖ్యతోపాటు ఎలక్ట్రాన్ గ్రాహ్య ఎంథాల్పీ అధిక రుణాత్మకమవుతుంది. పీరియడ్లో ఎడమ నుంచి కుడికి ప్రభావిత కేంద్రకావేశం పెరుగుతుంది. ఫలితంగా ఆవేశపు కేంద్రకానికి మొత్తం మీద చేరబోయే ఎలక్ట్రాన్ దగ్గరవుతుంది. కనుక చిన్న పరమాణువుకు ఎలక్ట్రాన్ ను కలపడం సులభం.
ప్రశ్న 94.
a) ఋణ విద్యుదాత్మకత అంటే ఏమిటి ?
b) గ్రూప్, పీరియడ్లో అది ఎట్లా మారుతుంది ?
జవాబు:
a) రసాయన పదార్థంలోని పరమాణువు సమిష్టిగా పంచుకున్న ఎలక్ట్రానులను తన వైపు ఆకర్షించుకునే ప్రవృత్తిని ఋణ విద్యుదాత్మకత అంటారు.
b) ఆవర్తనాపట్టికలో ఋణ విద్యుదాత్మకత పీరియడ్లో ఎడమ నుంచి కుడికి పెరుగుతుంది. ఉదా : లిథియం నుండి ఫ్లోరిన్కు పెరుగుతుంది. గ్రూపులో పై నుంచి కిందకి ఉదా : ఫ్లోరిన్ నుండి ఆస్టటైన్కు తగ్గుతుంది.
కారణం : గ్రూపులో పరమాణు పరిమాణం పెరగడం వల్ల ఋణవిద్యుదాత్మకతలు తగ్గుతాయి. అదే విధంగా పీరియడ్లో పరమాణు పరిమాణం తగ్గడం వల్ల ఋణ విద్యుదాత్మకత పెరుగుతుంది.
* ఋణ విద్యుదాత్మకతను పౌలింగ్ స్కేలులో కొలుస్తారు. బంధ శక్తుల ఆధారంగా కొలుస్తారు.
XA – XB \(0.208 \sqrt{\Delta}\)
XA = A యొక్క ఋణ విద్యుదాత్మకత
XB = B యొక్క ఋణ విద్యుదాత్మకత
Δ = బంధ ధృవాత్మకత
బంధ ధృవాత్మకత = ప్రయోగ బంధ శక్తి – సైద్ధాంతిక బంధ శక్తి
Δ = EA – B – \(\frac{1}{2}\)(EA – A + EB – B)
EA – B = A – B బంధశక్తి
EA – A = A – A బంధశక్తి
EB – B = B – B బంధశక్తి
లోహాలు ధన విద్యుదాత్మకతను చూపుతాయి. వాటి ఋణ విద్యుదాత్మకతలు తక్కువ. అలోహాలు అధిక ఋణ విద్యుదాత్మకతను కలిగి ఉంటాయి.
ప్రశ్న 95.
కింది వాటిని విశదీకరించండి.
a) సంయోజకత
b) కర్ణ సంబంధం
c) గ్రూప్ I లో ఆక్సైడ్ స్వభావంలో మార్పు.
జవాబు:
a) వేలన్సీ (సంయోజకత) అనగా సంయోజక శక్తి. ఏదైనా మూలక పరమాణువు ఎన్ని హైడ్రోజన్ పరమాణువులతో, లేదా క్లోరిన్ పరమాణువులతో కలుస్తోందో ఆ సంఖ్యను సంయోజకత అంటారు. సాధారణంగా ఒక గ్రూపులోని మూలకాలు ఒకే వేలన్సీని చూపుతాయి.
S బ్లాకు మూలకాలకు సంయోజకత గ్రూపు సంఖ్యకు సమానం.
p బ్లాకు మూలకాలకు సంయోజకత = గ్రూపు సంఖ్య లేదా (8 – గ్రూపు సంఖ్య)
హైడ్రోజన్ పరంగా వేలన్సీ : ప్రాతినిథ్య మూలకాలలో వేలన్సీ 1 నుండి 4 వరకు పెరిగి తరువాత 1 వరకు తగ్గుతుంది.
3వ పీరియడ్ మూలకాలు :

b) కర్ణ సంబంధం : ఇది రెండవ, మూడవ పీరియడ్లకు సంబంధించినది. ఆవర్తన పట్టికలో రెండో పీరియడ్లోని ఒక మూలకానికి మూడో పీరియడ్లోని తరువాత గ్రూపులోని రెండో మూలకానికి సారూప్య ధర్మాలుంటాయి. ఈ సంబంధాన్ని కర్ణ సంబంధం అంటారు.
ఉదా : Li, Mg; Be, Al; B, Si

c) గ్రూప్ I లో ఆక్సైడ్ స్వభావంలో మార్పు : గ్రూప్ I మూలకాలను ఆల్కలీ లోహాలు అంటారు. ఇవి క్షార ఆక్సైడ్లు.
ఇవి నీటిలో కరిగి క్షారాలను ఏర్పరుస్తాయి.
Na2O + H2O → 2 NaOH
గ్రూప్ I ఆక్సెడ్ క్షార ధర్మం Na2O నుండి Cs2O వరకు పెరుగుతుంది. దీనికి కారణం Na నుండి Cs వరకు లోహ స్వభావం పెరుగుటయే.
అదనపు ప్రశ్నలు
ప్రశ్న 1.
మనం మూలకలను ఎందుకు వర్గీకరించాలి ?
జవాబు:
మూలకాలను గురించిన అధ్యయనాన్ని సులభతరం చేయడం కోసం మూలకాలను వర్గీకరించాలి. మూలకాలు అధిక సంఖ్యలో ఉండుట వలన వాటి గురించి వాటి సమ్మేళనాల గురించి విడివిడిగా అధ్యయనం చేయడం చాలా కష్టం. ఈ సమస్యను అధిగమించడానికి శాస్త్రవేత్తలు మూలకాలను వర్గీకరించటం ద్వారా వాటి పరిజ్ఞానాన్ని పొందుపరచే ఒక క్రమ పద్ధతిని అన్వేషించారు. ఈ పద్ధతి మూలకాలను గురించి తెలిసిన రసాయన వాస్తవాలను హేతుబద్ధీకరించటమే కాకుండా తదుపరి అధ్యయనానికి కొత్త విషయాలను నిర్దేశిస్తుంది.
ప్రశ్న 2.
లాంథనమ్, d – బ్లాకుకు చెందిన మూలకం. f బ్లాకుకు చెందదు.
జవాబు:
ఆఫ్ సూత్రం ప్రకారం లాంథనమ్ ఎలక్ట్రాన్ విన్యాసం [Xe] 6s2 4f1. కాని భౌతిక పద్ధతుల విశ్లేషణ వల్ల [Xe] 6s2 5d1 గా కనుగొన్నారు. వేలన్సీ ఎలక్ట్రాన్ ఉపస్థాయిలో ఉన్నందున లాంథనమ్ను ‘d’ బ్లాకు మూలకంగా పరిగణిస్తారు.
ప్రశ్న 3.
Na2O నుంచి Cl2O7 వరకు పీరియడ్లో స్వభావం ఎట్లా మారుతుంది ?
జవాబు:
Na2O నుండి Cl2O7 వరకు ఆక్సైడ్స్లో క్షార స్వభావం తగ్గి ఆమ్ల స్వభావం పెరుగుతుంది.

ప్రశ్న 4.
ముల్లికెన్ స్కేలులో ఋణవిద్యుదాత్మకతను నిర్వచించండి.
జవాబు:
ముల్లికెన్ ప్రకారం, ఒక మూలకం ఋణవిద్యుదాత్మకత దాని అయనీకరణ శక్తి, ఎలక్ట్రాన్ అపేక్షల సగటు.

ప్రశ్న 5.
మెండలీవ్ ఆవర్తన నియమానికి ఏవైనా నాల్గు అవధులు చెప్పండి.
జవాబు:
మెండలీవ్ ఆవర్తన నియమానికి అవధులు :
- పరమాణు భారాల పరంగా లాంథనైడ్లోనే విరమృత్తిక మూలకాల స్థానాలను నిర్ణయించడం చాలా కష్టమవుతుంది. మెండలీవ్ ఆవర్తన పట్టికలో వీటన్నింటినీ ఒకే స్థానంలో ఉంచడం జరిగింది.
- ఈ పట్టికలో నాల్గు జతల మూలకాల్లో పరమాణు భారాల వరుసలు అపక్రమంలో ఉన్నాయి. అవి :
- ఆర్గాన్ – పొటాషియం
- కోబాల్డు – నికెల్
- టెల్యూరియం – అయొడిన్ మరియు
- థోరియం – ప్రోటాక్టినియంలు. కాని ఇవి మాత్రం పరమాణు సంఖ్యల ఆరోహణ క్రమంలోనే ఉన్నాయి.
- ఈ పట్టికలో కొన్ని మూలకాల స్థానాలు వాటి రసాయన గుణాలకు అనుగుణంగా లేవు. ఉదా : నాణెలోహాలైన Cu. Ag, Au లను అతిచురుకైన K, Rb. Cs అనే క్షార లోహాలతో కలిపి 1 గ్రూపులో ఉంచారు. ఈ రెండు సమూహాల మూలకాలకు ధర్మాలలో ఏ మాత్రం పోలికలు లేవు. ఉన్నదల్లా, వాటిన్నింటి వేలన్సీ సమానంగా ఉన్నది ( = 1)
- హైడ్రోజన్ ధర్మాలు మిగతా మూలకాల ధర్మాలతో అధికంగా పోలి ఉండవు. కొన్నిచర్యల్లో క్షార లోహాలను, మరికొన్ని చర్యల్లో హాలోజన్ అలోహాలను పోలి ఉంటుంది. కాబట్టి హైడ్రోజన్కు ఏ ఇతర మూలకానికీ లేని ప్రత్యేక స్థానాన్ని ఇచ్చారు.
- VIII వ గ్రూపులో మూడేసి లోహాలను కలిపి (త్రికము) ఒకే చోటు ఉంచారు. కారణం, రసాయనికంగా ఇవి అతి సన్నిహితత్వం చూపుతాయి.
ప్రశ్న 6.
ఉత్కృష్ట వాయుమూలకాలేవి ? ఆవర్తన పట్టికలోని వాటి స్థానాన్ని సమర్థించండి.
జవాబు:
సున్నా (0) గ్రూపు మూలకాలను ఉత్కృష్ట వాయువులంటారు. వీటినే జడవాయువులంటారు. అవి He, Ne, Ar, Kr, Xe మరియు Rn లు. ఈ మూలకాల ns మరియు np ఉపకక్ష్యలు పూర్తిగా నిండి ఉంటాయి. అనగా ns2 np6. (He కు 1s2) వీటి రసాయనిక జడత్వానికి కారణం, వీటిలోని బాహ్య కక్ష్య పూర్తిగా నిండి ఉండటమే. ఈ మూలకాలు ఏక పరమాణుక వాయువులుగానే ఉంటాయి.
ఈ మూలకాల విశిష్టత ఏమంటే, వీటి స్థిర విన్యాసం కారణంగా ఇవి అత్యధిక స్థిరమైనవిగా ఉంటాయి. వీటిని ఆవర్తన పట్టికలో కుడి చివరన p – బ్లాకులో ఉంచడానికి రెండు కారణాలున్నాయి. అవి
- వీనిలో, భేదాత్మక ఎలక్ట్రాన్ ఉపస్థాయిలోకి ప్రవేశిస్తుంది. (He కు తప్ప)
- ఈ మూలకాలు, VII A గ్రూపులోని అధిక ఋణవిద్యుదాత్మక హాలోజన్లకు, IA గ్రూపులోని అధిక ధనవిద్యుదాత్మక క్షారలోహాలకు మధ్యన వంతెన వలె నిలుస్తాయి.
ప్రశ్న 7.
d బ్లాకుకు చెంది పరివర్తన మూలకాలు కానివి ఏవి ?
జవాబు:
జింక్ (Zn), కాడ్మియం (Cd), మెర్కురీ (Hg)
ప్రశ్న 8.
ఎలక్ట్రాను అఫినిటీ, ఋణ విద్యుదాత్మకతల తేడా ఏమిటి ?
జవాబు:
ఎలక్ట్రాన్ అఫినిటీ ఒంటరి పరమాణువు ధర్మం, ఋణ విద్యుదాత్మకత బంధ గత పరమాణువు ధర్మం.
ప్రశ్న 9.
మిథ్యాజడవాయు విన్యాసం అంటే ఏమిటి ?
జవాబు:
బాహ్య కర్పరానికి ముందున్న కర్పరంలో s, p, dఉపస్థాయిలు నిండిన విన్యాసాన్ని సూడో (మిథ్యా) జడవాయు విన్యాసం అంటారు.
ఉదా : Zn++ [Ne] 3s2 3p6 3d10
ప్రశ్న 10.
ఆర్బిటాళ్లు చొచ్చుకొనిపోవటం అంటే ఏమిటి ?
జవాబు:
ఒక కక్ష్యలోని ఆర్బిటాల్, కేంద్రకం వైపుగా వెళ్లడాన్ని ఆర్బిటాల్ చొచ్చుకొని పోవడం అంటారు.
చొచ్చుకుపోయే క్రమం : s > p > d > f ఈ చొచ్చుకుపోయే సామర్థ్యము, ఆర్బిటాళ్ల ఆకృతులపైన ఆధారపడుతుంది.
ప్రశ్న 11.
విస్తృత ఆవర్తన పట్టిక యొక్క గొప్పదనాలు మరియు లోపాలు రాయండి.
జవాబు:
గొప్పదనాలు :
- “పరమాణు భారాల ఆరోహణ క్రమంలో అతిక్రమణ” అనే లోపం సరిదిద్దుకొన్నది.
- పట్టికలో మూలకం యొక్క స్థానాన్ని సులువుగా గుర్తించవచ్చు.
- మూలకాల ధర్మాలలో పోలికలు, భేదాలు మరియు క్రమమైన మార్పులు ఈ పట్టికలో స్పష్టంగా చిత్రీకరించబడ్డాయి.
- ట్రాన్షినల్ మూలకాలకు సరియైన స్థానం లభించింది.
- ఉప సమూహాలు (A మరియు B) విడివిడి గ్రూపులుగా లాజికల్గా వేరు చేయబడ్డాయి.
- జడవాయు మూలకాలను పట్టికలో కుడివైపు చిట్టచివర ఏర్పరచడం సంతృప్తికరంగా ఉంది.
లోపాలు :
- హైడ్రోజన్ యొక్క స్థానం సంతృప్తికరంగా లేదు.
- ప్రధాన పట్టికలో అంతర పరివర్తన మూలకాలకు స్థానం కల్పించలేదు. అవి పట్టికలో ప్రత్యేకంగా అడుగు భాగంలో ఏర్పాటు చేయబడ్డాయి.
- పరివర్తన మూలకాలను పొడుగు పీరియడ్లలో అమర్చడం వల్ల పొట్టి పీరియడ్ల మధ్య అంతరాయం ఏర్పడింది.
- Zn, Cd మరియు Hg ల స్థానం సంతృప్తికరంగా లేదు.
- VIIIవ గ్రూపులో మూడు ఉపసమూహాలు ఉండటం సరిగా లేదు.
- లోహాలు, ఆలోహాలు ప్రత్యేకంగా గుర్తింపబడలేదు.
ప్రశ్న 12.
ఋణ విద్యుదాత్మకతలకు పౌలింగ్ స్కేలు, ముల్లికెన్ స్కేలుకి గల సంబంధం వ్రాయండి.
జవాబు:
ముల్లికెన్ ఋణ విద్యుదాత్మకత = పౌలింగ్ ఋణ విద్యుదాత్మకత × 2,8
ప్రశ్న 13.
ఫ్లోరిన్కు ఋణ విద్యుదాత్మకత 4.0 అయితే ముల్లికెన్ స్కేలులో ఎంత ?
జవాబు:
(EN)M = (EN)P × 2.8
= (4.0) (2.8) = 11.2
ఏక సంయోజకతగల మూలకాలకు మాత్రమే ముల్లికెన్ స్కేలు నిర్వచనం వర్తిస్తుంది.
ప్రశ్న 14.
అత్యల్ప అయనీకరణ శక్తి కల మూలకం.
జవాబు:
సీసియం (Cs).